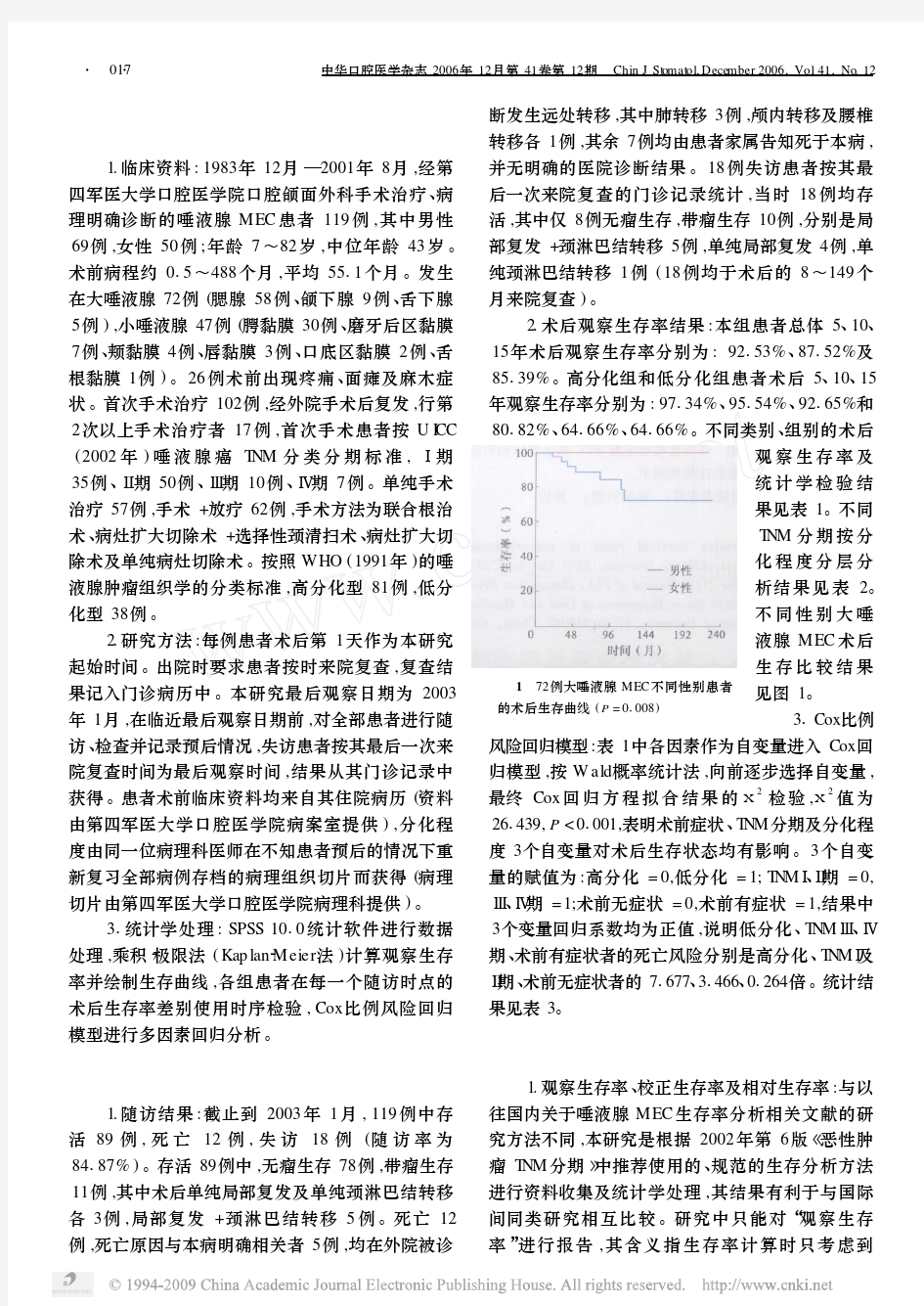
唾液腺黏液表皮样癌术后生存资料分析

34βe12、P63在涎腺黏液表皮样癌中的表达
目录 中文摘要 (Ⅰ) 英文摘要..............................................................................................................III 前言. (1) 1材料与方法 (3) 1.1实验材料 (3) 1.2主要仪器和设备 (3) 1.3实验方法 (4) 1.4免疫组化评分标准 (5) 2实验结果 (7) 2.1MEC病理组织学分型 (7) 2.234βe12和P63在NSG组和MEC组中的表达 (7) 2.334βe12和P63在不同的MEC组织病理学分型中的表达 (7) 2.434βe12和P63的表达与MEC临床表现的关系 (8) 3讨论 (10) 4结论 (13) 参考文献 (14) 综述 (17) 附录 (26) 致谢 (29) 在学期间承担/参与的科研课题与研究成果 (30) 个人简历 (31)
山西医科大学硕士学位论文 34βe12、P63在涎腺黏液表皮样癌中的表达 摘要 目的: 本实验通过采用免疫组织化学染色法,分别检测34βe12、P63在涎腺的正常组织(Normal salivary glands,NSG)和黏液表皮样癌(Mucoepidermoid Carcinoma,MEC)中的表达情况,以探讨二者在涎腺肿瘤发生发展中的作用及临床意义。 方法: 本实验的研究标本来自于山西医科大学第一医院病理科存档的手术切除的涎腺肿瘤组织的石蜡标本(时间为2006年1月-2014年1月),其中正常涎腺组织(NSG)为10例,黏液表皮样癌(MEC)为35例,采用免疫组化法分别检测二者在各组织块中的表达情况,所得的实验数据采用SPSS16.0软件进行统计学分析。 结果: (1)34βe12在10例NSG组中无表达,而在35例MEC组中有30例呈阳性表达,阳性率为85.7%,两者间差异具有统计学意义(P<0.01);34βe12在MEC的20例高分化组和15例低分化组中阳性表达数分别为16例(阳性率为80.0%)和14例(阳性率为93.3%),差异具有统计学意义(P<0.01);34βe12在31例无复发组中的阳性表达率为83.9%,4例复发组全部表达,复发组的34βe12阳性率显著高于无复发组(P<0.01);34βe12在31例无淋巴结转移组中的阳性表达率为83.9%,淋巴结转移组中4例全部表达,淋巴结转移组的34βe12阳性率显著高于无转移组(P<0.01);34βe12与黏液表皮样癌以肿瘤部位、性别、年龄各组之间的阳性表达率比较差异均无统计学意义(均P>0.05)。(2)P63在NSG组和MEC组中的阳性表达率分别为10%、71.4%,两者间差异具有统计学意义(P<0.01);P63在高分化组和低分化组中阳性表达例数分别为12例(阳性率为60.0%)和13例(阳 I
粘液表皮样癌
粘液表皮样癌 基本概述 粘液表皮样癌(mucoepidermoid carcinoma)也称粘液表皮样肿瘤(mucoepidermoid tumor),在涎腺肿瘤中占5%~10%。Stewart等根据其临床特点和组织学特征将其称为粘液表皮样肿瘤,并又分为良性及恶性两类。WHO也曾采用粘液表皮样瘤的名称,但以后许多学者认为这种命名分类并不恰当,认为此肿瘤全部为恶性,应称为粘液表皮样癌,并根据癌细胞分化程度的高低和生物学行为,将其分为低度恶性和高度恶性粘液表皮样癌。 WHO1990年修订的涎腺肿瘤的命名及分类已采用这种分类方法。虽然“粘液表皮样”一词并不完全合适,但基本上反映了肿瘤的主要成分为粘液样细胞和表皮样细胞。粘液表皮样癌来源于腺管的上皮细胞。[1] 发病原因 肿瘤的主要成分为粘液样细胞和表皮样细胞。粘液表皮样癌来源于腺管的上皮细胞。[2]临床表现 粘液表皮样癌发生在腮腺者最多,约占70%以上。小涎腺者常见于腭部,其他部位,如磨牙后区、颊部、上唇、下唇等部位则少有发生。可发生于任何年龄,以30~50岁多见,女性多于男性,约为1.5∶1。高分化者常呈无痛苦性肿块,生长缓慢。肿瘤大小不等,边界可清或不清,质地中等偏硬,表面可呈结节状。 腮腺肿瘤侵犯面神经时,可出现面瘫。手术后可以复发,但颈部淋巴结转移率低,血道转移更为少见。与高分化者相反,低分化黏液表皮样癌生长较快,可有疼痛,边界不清,与周围组织粘连。腮腺肿瘤常累及面神经,颈淋巴结转移率高,且可出现血到转移。术后易于复发。因此,高分化黏液表皮样癌术低度恶性肿瘤,而低分化黏液表皮样癌属高度恶性肿瘤。前者较常见,后者少见。 粘液表皮样癌的临床表现与临床的分化程度关系密切。高分化型,占多数,一般为无痛性肿块,生长较慢,病程较长。肿瘤体积大小不一,边界清楚,质偏硬,活动,表面光滑或呈结节状。可为囊性,亦可为实性。发生于腭部或磨牙后区者,可见肿块在粘膜下呈淡蓝色或暗紫色,粘膜光滑,质地软,穿刺可抽出少量血性紫黑色液体。 低分化型肿瘤生长较快,常伴疼痛。边界不清楚,呈弥散性,与周围组织有粘连,可破溃而继发感染,形成经久不愈的溃烂面,并有淡黄色粘稠分泌物。有时可形成涎瘘。发生于腮腺者,累及面神经时可发生面神经瘫痪症状及面肌抽搐症状。发生于腭部者,可能破坏硬腭。[3] 辅助检查
粘液表皮样癌是最常见的唾液腺恶性肿瘤
粘液表皮样癌是最常见的唾液腺恶性肿瘤。我们和其他人的研究共同表明,CRTC1-MAML2基因融合是临床病理学中常见的肿瘤特征之一。最近,在对粘液表皮样癌的研究中,科学家们报道了一种罕见的新型CRTC3-MAML2基因融合。这种新型的基因融合的发生频率和临床病理学意义尚不明朗。科学家们对101例粘液表皮样癌和89例非粘液表皮样癌的唾液标本进行了分析,并对被福尔马林固定和石蜡镶嵌过的标本进行了RNA提取。CRTC又分为分为CRTC1、CRTC2和CRTC3三种,我们对CRTC1-NAML2、CRTC2-NAML2和CRTC3-NAML2分别进行了RT-PCR检测,并从病人的临床记录中获得了其临床病理学数据。在101例粘液表皮样癌病例中,分别有34例和6例表现出CRTC1-NAML2和CRTC3-NAML2阳性。而在89例粘液表皮样癌病例中,则没有以上任何一种基因融合显示为阳性。在以往的病例分析中,我们知道CRTC1-NAML2和CRTC3-NAML2是相互排斥的,而CRTC2-NAML2则尚未被检测到。我们证实了CRTC1-NAML2阳性的粘液表皮样癌的临场病理学特征表现为惰性过程(indolent course)。而CRTC3-NAML2阳性的粘液表皮样癌的临场病理学特征则表现为进行肿瘤切除术后所有临场病例表现为低级的临床阶段(less-advanced clinic stage)、负节点新陈代谢过程(negative nodal metastasis)、无高阶肿瘤组织学(high-grade tumor histology)、无肿瘤再生或肿瘤
相关死亡。值得注意的是,CRTC3-NAML2患者的平均年龄(36岁)要远低于CRTC1-NAML2患者(55岁)和阴性患者(58岁)。综上所述,CRTC3-NAML2融合的发生概率被发现要高于较早研究的结果,对于存在CRTC3-NAML2融合的粘液表皮样癌常会伴随某些特定的临床病理学特征,且发病人群的平均年龄要远低于CRTC1-NAML2型或阴性粘液表皮样癌。
黏液表皮样癌(mucoepidermoid carcinoma,MEC)
黏液表皮样癌(mucoepidermoid carcinoma,MEC) 黏液表皮样癌是最常见的涎腺肿瘤,在大、小涎腺发生率相似。MEC 有3种类型细胞组成:黏液细胞通常较大和类似杯状,经常衬覆于囊壁;非角化表皮样细胞,甚至可能看起来是鳞状上皮;中间细胞则更像基底样或立方细胞。非典型性少见,表皮样/鳞状细胞倾向类似于正常黏膜上皮。 临床上,使用FISH检测MAML2重排对几种情况有帮助。在低级别MEC病例中,鉴别诊断需考虑良性肿瘤如Wathin瘤的化生性变型,或更罕见的疾病,如淋巴腺瘤。在这种情况下,对MAML2重排的检测可以确认MEC的诊断。在MEC 嗜酸细胞亚型的这种特殊情形中,MAML2 的FISH检测非常有用,因为其中突出的嗜酸细胞形态学可以掩盖表皮样表型,并类似WT、嗜酸细胞囊腺瘤或AciCC。虽然在许多情况下出现p63阳性反应提示MEC,但对MAML2重排的检测可确认MEC。尽管许多需与良性肿瘤(WT或嗜酸细胞囊腺瘤)鉴别的嗜酸细胞MEC 是低级别和转移风险较低,但恶性嗜酸细胞MEC由于复发风险较高,对其的诊断诊断仍很重要。 在瘤谱的另一端,高级别MEC可以类似各种其他高级别癌。在这种情况下MAML2重排的确定对MEC具有诊断性,而且可能很重要,因为在腮腺部位能排除转移的可能性。高级别MEC中的MAML2重排少见,因此没有重排也不能排除MEC的诊断。鉴别诊断需要考虑下列肿瘤,包括SDC、腺鳞癌、甚至鳞状细胞癌;一般而言,所有这些肿瘤都比高级别MEC预后更差。SDC通常由雄激素受体(AR)阳性而p63阴性,与MEC形成对照,后者通常为AR阴性,并至少具有p63的局灶阳性。腺鳞癌和鳞状细胞癌一般认为源自表面上皮,与MEC对比,后者没有表面原位癌成分。多灶角化的存在有利于鳞状细胞癌的诊断而非MEC。 MAML2基因断裂探针 探针应用 黏液表皮样癌有特征性的 t(11;19)易位,导致形成 MAML2-CRTC1 融合蛋白。MAML2重排在多达3/4的低级别和中级别MEC中被检测到,但是似乎不到一半的高级别MEC是重排阳性。 当 MEC 进行鉴别诊断时,将以 MAML2 的 FISH 检测作为涎腺肿瘤常见临床诊断有益的辅助手段。低级别MEC中,MAML2重排阳性提示 MEC而非 WT。MEC嗜酸细胞亚型中,复发风险较高,表型类似 WT、嗜酸细胞囊腺瘤或 AciCC,但MAML2重排阳性确诊为MEC。高级别 MEC 可以类似各种其他高级别癌,包括转移性鳞状细胞癌、腺鳞癌和 SDC,MAML2重排的确定对MEC具有诊断性。高级别 MEC 中的 MAML2 重排阴性不能排除MEC 的诊断。 MAML2 基因重排阳性患者具有较低的复发、转移和死亡率。 Notch 通路靶向治疗靶点。 订货信息 货号产品名称染料颜色供货周期FP-082 MAML2基因断裂探针红/绿非常规,两周 ·12·
涎腺粘液表皮样癌相关生物标志物研究进展
涎腺粘液表皮样癌相关生物标志物研究 进展 (作者:___________单位: ___________邮编: ___________) 【关键词】涎腺肿瘤流式细胞术血管内皮生长因子A 涎腺粘液表皮样癌(mucoepidermoid carcinoma)是口腔颌面部常见恶性肿瘤之一,它危害人类健康、威胁人类生命。根据国内六院校统计资料,在11947例涎腺上皮肿瘤中约占30%[1],可见于任何年龄,40~60岁为发病高峰。根据癌细胞分化程度和生物学特点,分为高分化(低度恶性)、中分化(中度恶性)和低分化(高度恶性)三型。当前,涎腺粘液表皮样癌的组织学诊断主要依靠HE染色切片,还没有一种用于诊断或估计预后的特异性标志物,因此研究用于涎腺粘液表皮样癌的诊断、预后和治疗特异性标志物就显得非常重要,随着肿瘤分子生物学领域的研究进展,一些新的生物标志物不断出现,不仅对涎腺粘液表皮样癌的病理诊断提供了帮助,并为其预后、治疗方案的选择提供了理论依据,在一定程度上发挥了独特作用[2]。但是目前,国内外所报道的涎腺粘液表皮样癌相关生物标志物较少,很多学者正在致力于对其的研究中。
1 肿瘤增殖标志物 肿瘤细胞DNA异倍体是恶性肿瘤细胞特征性标志之一,瘤细胞的增殖分数决定肿瘤的恶性程度,可以采用流式细胞术(flow cytometry,FCE)对癌细胞DNA倍体状态及其增殖分数进行分析,为患者的预后提供客观的信息[3]。Hicks等[4]对涎腺粘液表皮样癌预后因素进行研究时发现,涎腺粘液表皮样癌的增殖分数是评价其预后的明显因素。其他学者的研究表明,涎腺粘液表皮样癌细胞DNA倍体状态与复发及淋巴结转移密切相关。因此,DNA倍体和增殖分数的检测是研究涎腺粘液表皮样癌增殖状态的基本方法之一。 1.1 增殖细胞核抗原(Prolififerating cell nuclear antigen,PCNA)白,作为DNA聚合酶δ的辅助因子直接参与DNA的合成,对DNA复制的调节起重要作用。它在增殖细胞中表达最高,是评价细胞增殖状态的一个重要指标,与涎腺粘液表皮样癌的恶性程度及预后有关。在PCNA表达与涎腺粘液表皮样癌恶性程度相关性研究中,许多学者均发现涎腺粘液表皮样癌恶性程度与PCNA表达指数明显呈正相关[5,6]。Takahashi等[7]对27例腮腺肿瘤病人预后与PCNA表达指数之间的关系进行研究,将病人分为良性、低度恶性及高度恶性三组,高度恶性组的复发率和病死率明显高于良性和低度恶性组,结果发现相应的PCNA指数分别为0.7%、2%及23.1%,高度恶性组PCNA指数明显高于其他两组,故认为PCNA是决定腮腺肿瘤的预后的重要因素。 1.2 Ki67
