高中化学物质的溶解性表
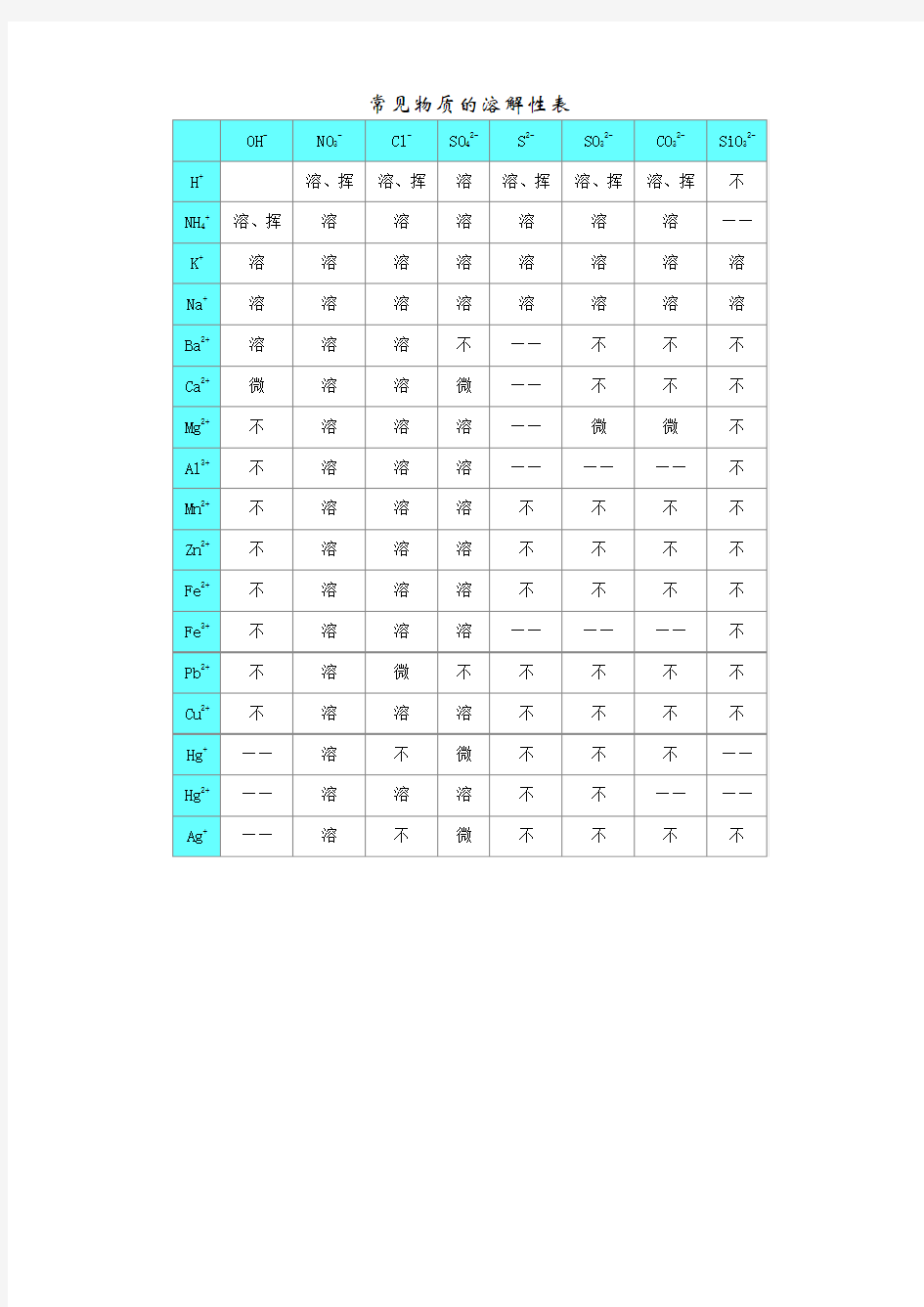
常见物质的溶解性表
初中化学:《物质的溶解性》教学设计1
《物质的溶解性》教学设计 【教学过程}一、导入: [教师演示]:汽油洗油漆的实验 提问:你知道汽油为什么能洗掉油漆吗? [学生回答]:是因为油漆能溶于汽油中 [教师问]:在生活中你对有关的物质溶解有什么现象和疑问吗? 二、[导出]新课《物质的溶解性》 学生提出疑问:如 1、在一定量的水中,不断增加蔗糖,蔗糖是否都能溶解? 2、例外物质的溶解能力相同吗? 3、物质的溶解能力是不变不变的吗? 4、蔗糖能溶解在所有的物质中吗? 5、气体能溶解在液体中吗? 6、物质溶解是从外界吸收热量,还是向外界放出热量? [教师]:我们这堂课就来解决以上这些问题。 [教师]:科学探究有那些步骤? [学生]:提出问题、建立假设、设计实验方案、收集证据、得出结论、成果交流[教师]:根据科学探究的过程,我们现在已经提出了问题,然后应该怎么办? [学生]:建立假设。 [教师提问]:你能假设吗?
[学生回答]: [教师]:建立假设以后又该如何呢? [学生回答]:设计实验 [教师]:如何设计呢? [学生回答]: [教师]:好,接下来我们就对第一个问题进行探究和收集证据 探索活动一(并完成表格):在一定量的水中,不断增加蔗糖,蔗糖是否都能溶解?学生得出结论:在一定条件下,物质能够溶解的数量是无限的。 [教师]:非常好,接下来我们进行第二个问题的探究和收集证据 探索活动二(并完成表格):例外物质的溶解能力相同吗? 学生得出结论:在相同条件下,例外物质的溶解能力例外的。 [教师]:非常好,接下来我们进行第三个问题的探究和收集证据 探索活动三(并完成表格):物质的溶解能力是不变不变的吗? 学生得出结论:蔗糖的溶解能力随温度的升高而增强。 [教师]:非常好,接下来我们进行第四个问题的探究和收集证据 探索活动四(并完成表格):蔗糖能溶解在所有的物质中吗? 学生得出结论:某物质在例外的其它物质中溶解能力也例外 [教师]:非常好,接下来我们进行第五个问题的探究和收集证据 探索活动五(并完成表格):气体能溶解在液体中吗? 学生得出结论:气体能溶解在液体中,并随着温度的升高,气体的溶解能力逐渐减弱,所以大量气泡从水中冒出。
教案精选初三化学《物质的溶解性》教学设计
教案精选:初三化学《物质的溶解性》教学 设计 教案精选:初三化学《物质的溶解性》教学设计教学目标 知识目标: 1.使学生理解的概念,了解温度对一些固体物质的影响;了解曲线的意义; 2.使学生对气体受温度、压强的影响关系,有一个大致的印象; 3.使学生掌握有关的几种基本计算。 能力目标: 会利用曲线查找常见物质在一定温度下的和随温度变化的趋势。 情感目标: 通过对不同物质的比较和外界条件对物质的影响的分析,体会事物内外因关系和质变与量变辩证关系。 教学建议 关于曲线的意义 固体物质的随温度变化有两种表示方法,一种是列表法,如教材中表7-1;另一种是坐标法,即在直角坐标系上
画出坐标曲线,如课本图7-1。可以先向学生说明曲线绘制原理(不要求学生绘制),再举例讲解如何应用这种曲线图。 固体的曲线可以表示如下几种关系: (1)同一物质在不同温度时的不同的数值; (2)不同物质在同一温度时的数值; (3)物质的受温度变化影响的大小; (4)比较某一温度下各种物质的大小等。 进行这些分析之后,教师还可以就某物质在曲线上的任一点,请同学回答其表示的含义,来验证学生是否已了解曲线。例如,横坐标是60,纵坐标是110的点表示什么含义。学生应该回答(1)代表60℃时硝酸钾在水中的是110克;(2)代表60℃时,100克水里,达到饱和时可溶解硝酸钾100克等等。当然,可以提出教材中表7-l中未列出的温度,例如让学生说出35℃时硝酸钾的是多少,这时学生可以利用曲线顺利地作出回答,使学生体会到曲线图在这方面所表现的特点。 关于溶解性和的区别与联系 物质的溶解性与物质的之间,既有联系,又有区别。为了使学生深刻理解的概念,就必须先了解物质溶解性的知识,在教学中要帮助学生区分这两个概念。 物质的溶解性,即物质溶解能力的大小。这种能力既取决于溶质的本性,又取决于它跟溶剂之间的关系。不论其原
物质的溶解性
§6-3物质的溶解性 一、素质教育目标: (一)知识目标 1.通过三组探究实验了解影响物质溶解性的三个因素:溶质与溶剂的本身性质和温度。 2.通过探究活动了解饱和溶液与不饱和溶液的概念,并与日常生活为基础,交流讨论饱和溶液与不饱和溶液的相互转化的方法。 3.在学习溶解性和饱和溶液的基础上继续学习并知道物质溶解性的定量表示(固体溶解度的概念),影响固体溶解度的因素,并知道可以用固体溶解度曲线表示某物质在一定温度时的溶解度。 4.学习描绘固体溶解度曲线,并能利用它解决一些问题。 5.稍微了解气体溶解度的有关情况。 6.通过探究活动了解结晶现象并知道结晶在生产生活中的广泛应用。 (二)能力目标 1.培养学生通过实验解决问题的能力,更突出的是培养学生在实验基础上的分析能力和思维能力。 2.利用实验和数据的结合,培养学生区分不同概念的比较能力和分析思维能力。 3.培养学生识图和用图解决一些问题的能力。 4.培养学生实验操作能力,以及他们对实验过程和实验结果的表述能力。 (三)德育目标 1.通过对实验的分析研究,培养学生沿着“问题—实验探究—分析—结论”的思路,以科学的方法去解决问题的能力。 2.通过探究与讨论,发展同学们合作学习、勤于思考、严谨求实、勇于实践的科学精神。二、重点: 1.建立溶解性、溶解度、饱和溶液与不饱和溶液、结晶的概念 2.知道饱和溶液与不饱和溶液相互转化的方法。 3.知道影响物质溶解性和固体溶解度的因素。 4.了解固体溶解度曲线的意义并学习描绘和使用固体溶解度曲线。 5.利用结晶方法,分离几种可溶性物质的混合物的原理。 三、难点: 1.正确理解物质溶解性的定量表示——溶解度的概念,区分溶解性与溶解度在概念上的不同。 2.饱和溶液与不饱和溶液相互转化的方法。 3.描绘和使用固体溶解度曲线。 4.利用结晶方法,分离几种可溶性固体物质的混合物的原理。 四、课时安排:3课时。 五、课前准备: 教师准备: (物质)投影仪、电脑、(分组实验用品)食盐、蔗糖、消石灰、水、汽油、食用油、硝酸钾、 饱和蔗糖水溶液、试管、烧杯、酒精灯、滴管、水槽、玻璃片、玻璃棒、硫酸亚铁晶体、硫酸 铜晶体、硝酸钾晶体、重铬酸钾晶体、温度计、移液管、铁架台、 (知识)有关有机溶剂的知识、干洗原理、血渍清洗知识、油笔芯清洗知识 学生准备: 小实验与社会实践 1.小实验
“物质的溶解性”的教学设计新部编版
教师学科教案[ 20 – 20 学年度第__学期] 任教学科:_____________ 任教年级:_____________ 任教老师:_____________ xx市实验学校
《物质的溶解性》教学设计 华师大张江实验中学马金凤 一、设计说明 学习物质的溶解性是为学习溶解度、溶质质量分数等基本概念作必要准备。在以往的教学中,按照书上的内容设置往往要通过两节课甚至更多时间才能完成,本节课的两个实验原理比较简单但操作却耗时较多,基于对“溶液”主题单元的思考,对本节课的课时教学内容(包括实验)做了调整,期待提高“溶液”单元整体教学的有效性。 本节课设想充分利用学生已有关于物质溶解现象的经验,将课本中的课堂实验一设计成简单可行的家庭试验(如比较白糖和面粉的溶解性大小),既节省课堂时间,也为学生的自主探究创造了条件。课堂上进行的实验,则是大多数学生没有条件在课外亲身感受的部分(如不同溶剂对物质溶解性的影响)。对于课堂实验,要精心设计,使其充分发挥功能:既让学生感知实验事实或变化规律,更要有利于学生在实验事实的基础上逐步构建概念知识,将感性认识上升为理性认知,完成知识的内化过程,也巧妙地使教学过程逐步推进,在有限的时间里有序高效地完成“繁多”的教学内容。本节课中的实验,以尽可能少的药品和仪器装置,尽可能简单的操作步骤,实现了多重功能(认识溶剂对物质溶解性的影响,饱和溶液概念的建构,感知饱和溶液和不饱和溶液相互转化的方法,培养学生设计实验的能力、实验基本操作能力及合作精神等)。 二、教材的地位和作用 学生在六、七年级《科学》中学习过物质的溶解、溶液由溶质和溶剂组成等知识,同时在日常生活中,学生有意无意地知道一些物质可以溶解在其他物质中,比较清楚地知道大多数物质可以在水中溶解,但对一些物质在一定条件下不能无限制溶解,各种物质在相同条件下溶解的能力并不同,某种物质的溶解能力与外界条件有关,液体和气体的溶解情况等还是比较模糊,缺乏系统的整理。通过本节课知识(影响物质溶解性的因素)的学习为后面知识(物质溶解性的定量表示等)的学习作好铺垫。
初中化学方程式汇总及物质溶解性表
初中化学方程式汇总 化合反应 1、镁在空气中燃烧:2Mg + O2点燃 2MgO 2、铁在氧气中燃烧:3Fe + 2O2点燃 Fe3O4 3、铝在空气中燃烧:4Al + 3O2点燃 2Al2O3 4、氢气在空气中燃烧:2H2 + O2点燃 2H2O 5、红磷在空气中燃烧:4P + 5O2点燃 2P2O5 6、硫粉在空气中燃烧: S + O2点燃 SO2 7、碳在氧气中充分燃烧:C + O2点燃 CO2 8、碳在氧气中不充分燃烧:2C + O2点燃 2CO 9、二氧化碳通过灼热碳层: C + CO2高温 2CO 10、一氧化碳在氧气中燃烧:2CO + O2 点燃 2CO2 12、生石灰溶于水:CaO + H2O === Ca(OH)2 13、无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4?5H2O 14、钠在氯气中燃烧:2Na + Cl2点燃 2NaCl 15、无水硫酸铜作干燥剂:CuSO4 + 5H2O ==== CuSO4?5H2 16、二氧化碳和水反应(二氧化碳通入紫色石蕊试液):CO2+ H2O === H2CO317、生石灰溶于水:CaO + H2O === Ca(OH)2 18、氧化钠溶于水:Na2O + H2O ==== 2NaOH 19、三氧化硫溶于水:SO3 + H2O ==== H2SO4 分解反应 20、实验室用双氧水制氧气:2H2O2 2H2O+ O2↑ 21、加热高锰酸钾:2KMnO4△2MnO4 + MnO2 + O2↑ 22、加热氯酸钾 2KClO3△2 23、水在直流电的作用下分解:2H2O通电2H2↑+ O2↑ 24、碳酸不稳定而分解:H2CO3 === H2O + CO2↑ 25、高温煅烧石灰石(二氧化碳工业制法):CaCO3高温 CaO + CO2↑ 26、加热碱式碳酸铜:Cu2(OH)2CO3△2O + CO2↑ 27、硫酸铜晶体受热分解:CuSO4?5H2O△CuSO4 + 5H2O 置换反应 (1)单质与氧化物反应 28、氢气还原氧化铜:H2 + CuO △2O 29、木炭还原氧化铜:C+ 2CuO 高温 2Cu + CO2↑ 30、水蒸气通过灼热碳层:H2O + C 高温 H2 + CO
化学常见常见沉淀及溶解性口诀
常见沉淀 白色: BaSO4/BaCO3/CaCO3/AgCl/Ag2CO3/Mg(OH)2/Fe(OH)2/Al(OH)3/CuCO3/ZnCO3/MnCO3/ Zn(OH)2 Fe(OH)2 蓝色:Cu(OH)2 浅黄色:AgBr 红褐色:Fe(OH)3 沉淀鉴别 Cu(OH)2蓝色沉淀Fe(OH)3红褐色沉淀AgBr淡黄色沉淀AgI ,Ag3PO4黄色沉淀CuO 黑色沉淀Cu2O 红色沉淀Fe2O3 红棕色沉淀FeO 黑色沉淀FeS2 黄色沉淀PbS 黑色沉淀FeCO3 灰色沉淀Ag2CO3 黄色沉淀AgBr 浅黄色沉淀AgCl 白色沉淀Cu2(OH)2CO3 暗绿色沉淀BaCO3白色沉淀(且有CO2生成)CaCO3白色沉淀(且有CO2生成)BaSO4白色沉淀不溶的碳酸盐白色沉淀(且有CO2生成)不溶的碱、金属氧化物白色沉淀(且有CO2生成)Fe(OH)2为白色絮状沉淀(在空气中很快变成灰绿色,再变成Fe(OH)3红褐色沉淀) 相关口诀 钾钠铵盐硝酸盐均可溶 盐酸盐银不溶 硫酸盐钡不溶 白色沉淀: CaCO3. BaCO3 . BaSO4. AgCL. Mg(OH)2 蓝色沉淀: Cu(OH)2 红褐色沉淀: Fe(OH)3 不建议死记硬背,只需记住每个阴离子里哪个不溶即可,钾钠铵硝都溶 溶解性口诀一 钾钠铵盐溶水快,① 硫酸盐除去钡银铅钙。② 氯化物不溶氯化银,
硝酸盐溶液都透明。③ 氢氧根多溶一个钡④ 口诀中未有皆下沉。⑤ 注: ①钾钠铵盐都溶于水; ②硫酸盐中只有硫酸钡、硫酸铅不溶(硫酸钙硫酸银微溶也是沉淀); ③硝酸盐都溶于水; ④碱性物质中除了钾离子钠离子铵离子锂离子还有钡离子也可溶 ⑤口诀中没有涉及的盐类都不溶于水; 溶解性口诀二 钾、钠、铵盐、硝酸盐; 氯化物除银、亚汞; 硫酸盐除钡和铅; 碳酸、磷酸盐,只溶钾、钠、铵。 说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。 溶解性口诀三 钾钠铵硝皆可溶、盐酸盐不溶银亚汞; 硫酸盐不溶钡和铅、碳磷酸盐多不溶。 多数酸溶碱少溶、只有钾钠铵钡溶 溶解性口诀四 钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。) 盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。) 再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。) 其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物) 只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶) 最后说碱类,钾、钠、铵和钡。(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶)另有几种微溶物,可单独记住。
九年级化学--物质的溶解性练习(含答案)
九年级化学--物质的溶解性练习(含答案) 夯实基础 1.已知20 ℃时,氯化钠的溶解度为36 g。此时,20 g水中最多能溶解氯化钠的质量为( ) A.36 g B.3.6 g C.7.2 g D.10 g 2.现有一杯20 ℃的硝酸钾不饱和溶液,能改变硝酸钾溶解度的操作是( ) A.加硝酸钾 B.充分搅拌 C.恒温蒸发水 D.升高温度 3.在粗盐的初步提纯实验中,下列操作正确的是( ) 图K13-1 4.在粗盐提纯的实验操作中,下列说法正确的是( ) A.过滤时用到的仪器:烧杯、玻璃棒、铁架台、滤纸 B.蒸发操作结束后,将蒸发皿放在石棉网上 C.用药匙将蒸发皿中的白色固体直接转移到纸上 D.实验结束后所得到的白色固体为氯化钠 5.硝酸钾在不同温度下的溶解度数据如下表。下列说法错误的是( ) A. B.60 ℃时,饱和硝酸钾溶液中溶质与溶液的质量之比为11∶21 C.20 ℃时,10 g水中加入5 g硝酸钾充分溶解后再加入5 g水,前后溶质的质量分数不变 D.将溶质质量分数为28%的硝酸钾溶液从60 ℃降温至20 ℃,没有晶体析出
6. 图K13-2 甲、乙的溶解度曲线如图K13-2所示。下列有关说法不正确的是( ) A.t 2 ℃时,甲的饱和溶液中溶质和溶剂的质量之比为2∶5 B.t 2℃时,乙的饱和溶液降温到t 1 ℃后,溶液仍饱和 C.t 1 ℃时,甲、乙两种饱和溶液中溶质的质量相等 D.甲、乙的饱和溶液分别从t 2℃降温到t 1 ℃,两溶液中溶质质量分数相等 7.某盐化工厂生产的碳酸钠粗产品中含有少量的氯化钠。碳酸钠和氯化钠的溶解度与温度的关系如图K13-3所示,请回答: 图K13-3 (1)t 1 ℃时碳酸钠与氯化钠中溶解度较大的物质是____________________。 (2)t 1℃时碳酸钠溶液升温至t 2 ℃,所得溶液的溶质质量分数________(填“变大”“变 小”或“不变”)。 (3)除去碳酸钠中混有的少量氯化钠的方法是________________。 8.根据下表中氯化钠和硝酸钾部分溶解度数据分析回答下列问题。
物质的溶解度
溶解度计算1 姓名_________ 1、把50克20℃时的硝酸钾饱和溶液蒸干,得到12克硝酸钾。求20℃时硝酸钾的溶解度。 2、 70℃时,硝酸钾的溶解度为138克,配制饱和溶液时: (1)60克水最少需要加入硝酸钾多少克。 (2)13.8克硝酸钾最多可加入水多少克。 (3)70℃100克的硝酸钾饱和溶液里含硝酸钾多少克。 3、80℃时,硝酸钾的溶解度为169克,在此温度下将90.2克的硝酸钾溶解在60克水里,计算: (1)此溶液是饱和溶液还是不饱和溶液? (2)若用蒸发溶剂的方法使其达到饱和,需要蒸发多少克水? (3)若用增加溶质的方法使其达到饱和,应再加入硝酸钾多少克? 4、60℃时90克KNO3固体加入75克水后充分振荡,有7.5克没有溶解。求60℃时KNO3的溶解度。 5、已知60℃时溶解度为110克,有90克KNO3固体,加入75克水,能得到多少克溶液? 6、20℃,氯化钠的溶解度为36克。 (1)20℃,氯化钠溶液中有部分晶体未溶,加入25克水恰好将其溶解,问没有溶解的晶体有多少克? (2)将20℃氯化钠饱和溶液34克蒸干,可以得到晶体多少克? 8、20度时,50gA溶于水,形成200g不饱和溶液,现蒸发原水量的一半,溶液刚好达到饱和,求20度时A的溶解度。 9、20度时,已知氯化钠的溶解度时36g,现有27g食盐溶解在该温度下的200g水中,要使溶液达到饱和状态,问:(1)至少需要加入食盐多少克?(2)至少需要蒸发水多少克?10、20度时,将某固体物质60g完全溶解于水,制成200ml密度为1.5g/ml的饱和溶液,求20度时该物质的溶解度。 11、20度时,227g不饱和溶液,如果加入45g某物质或蒸发125g水都能达到饱和,则20度时该物质的溶解度时多少克? 12、一定温度下,Ag某固体溶质加入水中,制成Bg该溶质的饱和溶液,该物质在此温度下的溶解度是多少? 13、T度时的硝酸钾溶液200g,蒸发掉10g水后析出晶体4g,又蒸发10g水后析出晶体6g,再蒸发20g水析出晶体的质量是________________。 14、25℃时,M固体(硝酸钾)的溶液200克,当温度不变,蒸发掉20克水时,有5克M 析出;若再蒸发掉20克水时,有10克M析出;若又蒸发掉20克水时,可析出M物质的质量是_____,则25℃时M物质的溶解度______。 15、已知25℃时,50克水中需溶解12.5克硝酸钾才能达到饱和。现有一杯硝酸钾溶液500克,若要使其达到饱和需蒸发10克水,若改用加硝酸钾的方法,需加_____克硝酸钾才能使其达到饱和? 16、 30℃时,将A物质的溶液平均分成二等份,第一份恒温蒸发10克水,有1克A析出,第二次恒温蒸发25克水,有5克A析出,若第一份继续蒸发15克水,有____克晶体析出.则30℃时,A物质的溶解度为_______. 17、某温度下,将A物质的水溶液分成等量的2份,向第一份中加入9克A物质,充分搅拌,尚有1克固体不能溶解,将第二份溶液蒸发掉40克水,并恢复到原温度,溶液恰好饱和(无A析出),则A物质在该温度下的溶解度是_______。
物质溶解度表汇总
1.锕、氨、铵 物质化学式0℃10℃20℃30℃40℃50℃60℃70℃80℃90℃100℃氢氧化锕Ac(OH)3 0.0022 氨NH3 88.5 70 56 44.5 34 36.5 20 15 11 8 7 叠氮化氨NH2N2 16 25.3 37.1 苯甲酸氨NH4C7H5O2 20 碳酸氢氨NH4CO3 11.9 16.1 21.7 28.4 36.6 59.2 109 170 354 溴化氨NH4Br 60.6 68.1 76.4 83.2 91.2 108 125 135 145 碳酸氨(NH4)2CO3100 氯酸氨NH4ClO328.7 氯化氨NH4Cl 29.4 33.2 37.2 41.4 45.8 50.4 55.3 60.2 65.6 71.2 77.3 氯铂酸铵(NH4)2PtCl60.289 0.374 0.499 0.637 0.815 1.44 2.16 2.61 3.36 铬酸铵(NH4)2CrO425 29.2 34 39.3 45.3 59 76.1 重铬酸铵(NH4)2Cr2O718.2 25.5 35.6 46.5 58.5 86 115 156 砷酸二氢铵NH4H2AsO433.7 48.7 63.8 83 107 122 磷酸二氢铵NH4H2PO422.7 39.5 37.4 46.4 56.7 82.5 118 173 氟硅酸铵(NH4)2SiF6 18.6 甲酸铵NH4HCO2 102 143 204 311 533 磷酸一氢铵(NH4)2HPO4 42.9 62.9 68.9 75.1 81.8 97.2 碳酸氢铵NH4HSO4 100 酒石酸氢铵NH4HC4H4O6 1.88 2.7 碘酸铵NH4IO3 2.6 碘化铵NH4I 155 163 172 182 191 209 229 250 硝酸铵NH4NO3 118 150 192 242 297 421 580 740 871 高碘酸铵(NH4)5IO6 2.7 草酸铵(NH4)2C2O4 2.2 3.21 4.45 6.09 8.18 14 22.4 27.9 34.7 高氯酸铵NH4ClO4 12 16.4 21.7 37.7 34.6 49.9 68.9 高锰酸铵NH4MnO4 0.8 磷酸铵(NH4)3PO4 26.1 硒酸铵(NH4)2SeO4 96 105 115 126 143 192 硫酸铵(NH4)2SO4 70.6 73 75.4 78 81 88 95 103 亚硫酸铵(NH4)2SO3 47.9 54 60.8 68.8 78.4 104 114 150 153 酒石酸铵(NH4)2C4H4O6 45 55 63 70.5 76.5 86.9 硫氰酸铵NH4SCN 120 144 170 208 234 346 硫代硫酸铵(NH4)2S2O3 2.15 钒酸铵NH4VO3 0.48 0.84 1.32 2.42
高中化学常用物质溶解性表及沉淀颜色
高中化学常用物质溶解性表及沉淀颜色 Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解溶液呈黄色铁器除锈 AI2O3+3H2SO4= AI2(SO4)3+3H2O 白色固体溶解 CuO+H2SO4=CuSO4+H2O 黑色固体溶解溶液呈蓝色 ZnO+H2SO4=Z nSO4+H2O 白色固体溶解 MgO+H2SO4=MgSO4+H2O 白色固体溶解 2NaOH+H2SO4=Na2SO4+2H2O Cu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解 Ca(OH)2+H2SO4=CaSO4+2H2O Mg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解 2AI(OH)3+3H2SO4=AI2(SO4)3+3H2O 白色固体溶解 2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解溶液呈黄色 Ba(OH)2+ H2SO4=BaSO4+2H2O 生成白色沉淀不溶解于稀硝酸 检验 SO42的原理 BaCI2+ H2SO4=BaSO4+2HCI 生成白色沉淀不溶解于稀硝酸检验SO42 的原理 Ba(NO3)2+H2SO4=BaSO4+2HNO3 生成白色沉淀不溶解于稀硝酸 检验 SO42的原理 Na2O+2HNO3=2NaNO3+H2O CuO+2HNO3=Cu(NO3)2+H2O ZnO+2HNO3=Z n(NO3)2+ H2O MgO+2HNO3=Mg(NO3)2+ H2O CaO+2HNO3=Ca(NO3)2+ H2O NaOH+HNO3=NaNO3+ H2O Cu(OH)2+2HNO3=Cu(NO3)2+2H2O Mg(OH)2+2HNO3=Mg(NO3)2+2H2O AI(OH)3+3HNO3=AI(NO3)3+3H2O Ca(OH)2+2HNO3=Ca(NO3)2+2H2O Fe(OH)3+3HNO3=Fe(NO3)3+3H2O 3NaOH + H3PO4=3H2O + Na3PO4 白色固体溶解 黑色固体溶解溶液呈蓝色 白色固体溶解 白色固体溶解 白色固体溶解 蓝色固体溶解 白色固体溶解 白色固体溶解 红褐色沉淀溶解溶液呈黄色
初中化学中常见物质的溶解性情况
初中化学中常见物质的溶解性情况 单质 1、【金属单质 ....】:所有金属几乎难溶于水(但一些金属由于很活泼,在常温下能够和水发生反应:例如K、Ca、Na等)。 2、【非金属单质 .....】:①(固态)C、S、P等难溶于水; ②(气态) N2、H2 等难溶于水,O2 不易溶于水。 化合物 1、【酸的溶解性 .....】 【大部分酸及酸性氧化物(非金属氧化物)能溶于水,(酸性氧化物+水→酸)大部分碱性氧化物(金属氧化物)不溶于水,能溶的有:氧化钡、氧化钾、氧化钙、氧化钠(碱性氧化物+水→碱)】。 2、【碱的溶解性 .....】 ▲溶于水的碱有:氢氧化钡、氢氧化钾、氢氧化钠和氨水。▲其他的碱大部分不溶于水:难溶性碱中Fe(OH)3是红褐色沉淀,Cu(OH)2是蓝色沉淀,其他难溶性碱为白色(包括Fe(OH)2)。 ▲其中AgOH 为白色固体,属于碱,常温下AgOH极不稳
定,易分解为棕褐色难溶于水的氧化银固体.低温下可制得氢氧化银在水中的白色沉淀,Ca(OH)2为微溶于水的白色固体。 3、【盐的溶解性 .....】 ★含有钾、钠、硝酸根、铵根的物质都溶于水; ★含Cl- 的化合物只有AgCl不溶于水,其他都溶于水;★含SO42-的化合物只有BaSO4不溶于水,Ag2SO4、CaSO4微溶于水, 其他都溶于水; ★含CO32-的物质只有K2CO3、Na2CO3、(NH4)2CO3溶于水,其他绝大部分不溶于水,一些微溶于水或者遇到水发生水解。注意:【沉淀物中AgCl和BaSO4不溶于稀硝酸,其他沉淀物能溶于酸。如:Mg(OH)2、CaCO3、BaCO3、Ag2 CO3等】 4、【氧化物的溶解性 .......】 ▲金属氧化物一般都不溶解,例如:CuO, Fe2O3, Fe3O4 ,MgO, Al2O3 ,MnO2等, 其中CaO能与水反应。 ▲非金属氧化物:①难溶于水,例如:CO、NO等。 ②可溶于水,例如:CO2(其中CO2 溶于水后又能与水反应)。 ③易溶于水:例如:SO2、NO2等。 5、【其他 ......】 ..物质的溶解性 ▲①难溶于水:CH4 ;②易溶于水: HCl、NH3 (其中NH3溶于水后又能与水反应)、葡萄糖、蔗糖等。
常见物质溶解性及溶度积
本溶解性表崔扬(vmbn)录入,2003-5-5,修正于2003-7-27
]锕、氨、铵 物质化学式0°C10°C20°C30°C40°C50°C60°C70°C80°C90°C100°C 氢氧化锕(III)Ac(OH) 3 0.0022 氨NH 3 88.5 70 56 44.5 34 26.5 20 15 11 8 7 叠氮化铵NH 4N 3 16 25.3 37.1 苯甲酸铵NH 4C 7 H 5 O 2 20 碳酸氢铵NH 4HCO 3 11.9 16.1 21.7 28.4 36.6 59.2 109 170 354 溴化铵NH 4 Br60.6 68.1 76.4 83.2 91.2 108 125 135 145 碳酸铵(NH 4) 2 CO 3 100 氯酸铵NH 4ClO 3 28.7 氯化铵NH 4 Cl29.4 33.2 37.2 41.4 45.8 50.4 55.3 60.2 65.6 71.2 77.3 氯铂酸铵(NH 4) 2 PtCl 6 0.289 0.374 0.499 0.637 0.815 1.44 2.16 2.61 3.36
铬酸铵(NH 4) 2 CrO 4 25 29.2 34 39.3 45.3 59 76.1 重铬酸铵(NH 4) 2 Cr 2 O 7 18.2 25.5 35.6 46.5 58.5 86 115 156 砷酸二氢铵NH 4H 2 AsO 4 33.7 48.7 63.8 83 107 122 磷酸二氢铵NH 4H 2 PO 4 22.7 39.5 37.4 46.4 56.7 82.5 118 173 氟硅酸铵(NH 4) 2 SiF 6 18.6 甲酸铵NH 4HCO 2 102 143 204 311 533 磷酸一氢铵(NH 4) 2 HPO 4 42.9 62.9 68.9 75.1 81.8 97.2 硫酸氢铵NH 4HSO 4 100 酒石酸氢铵NH 4HC 4 H 4 O 6 1.88 2.7 碘酸铵NH 4IO 3 2.6 碘化铵NH 4 I155 163 172 182 191 209 229 250 硝酸铵NH 4NO 3 118 150 192 242 297 421 580 740 871
常见物质溶解性及溶度积_图文(精)
常见物质溶解性 Ag+Hg22+Pb2+Hg2+Bi3+Cu2+Cd2+As3+Sb3+Sn2+Sn4+Al3+Cr3+Fe3+Fe2+Mn 2+Ni2+Co2+Zn2+Ba2+Sr2+Ca2+Mg2+K+Na+NH4+碳酸盐, CO32- HNO3HNO3HNO3HCl HCl HCl HCl -------HCl HCl HCl HCl HCl HCl HCl HCl 略溶水水水草酸盐,C2O42-HNO3HNO3HNO3HCl HCl HCl HCl -HCl HCl 水HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl 水水水水 氟化物, F-水水略溶, HNO3 水HCl 略溶, HCl 略溶, HCl - 略溶, HCl 水水水水 略溶, HCl 略溶,
HCl HCl HCl HCl HCl 略溶HCl 不溶HCl 水水水 亚硫酸盐, SO32-HNO3HNO3HNO3HCl -HCl HCl --HCl -HCl --HCl HCl HCl HCl HCl HCl HCl HCl 水水水水AsO33-HNO3HNO3HNO3HCl HCl HCl HCl --HCl ---HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl 水水水AsO43-HNO3HNO3HNO3HCl HCl HCl HCl --HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl 水水水磷酸盐, PO43-HNO3HNO3HNO3HCl HCl HCl HCl -HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl 水水水BO2-HNO3-HNO3-HCl HCl HCl --HCl -HCl HCl HCl HCl HCl HCl HCl HCl HCl 略溶略溶HCl 水水水硅酸盐, SiO32-HNO3-HNO3-HCl HCl HCl ----HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl HCl 水水水 酒石酸, C4H4O62-HNO3略溶, HNO3 HNO3HCl HCl 水HCl -HCl HCl 水水水水HCl 略溶, HCl HCl 水HCl HCl HCl HCl 水水水水 硫酸盐, SO42-略溶略溶不溶略溶略溶水水-HCl 水-水水水水水水水水不溶不溶微溶水水水水 CrO4-HNO3HNO3HNO3HCl HCl 水HCl --HCl --HCl 水-略溶, HCl HCl HCl 水HCl 略溶水水水水水
一些物质的溶解度
硫代硫酸钠:0℃50.2、10℃59.7、20℃70.1、30℃82.2、40℃105、50℃142、60℃191、80℃231、100℃245 (25℃75.9); 硫代硫酸钠?5水:0℃ 52.5、10℃ 61.0、20℃ 70.0、30℃ 84.7、40℃ 103、50℃ 170、60℃ 207、80℃ 249、90℃ 254、100℃ 266。 氢氧化钠 温度0 10 20 30 40 50 60 70 80 90 100 溶解度g 42 51 109 119 129 145 174 299 314 329 347 碳酸钠 在35.4℃其溶解度最大,每100g水中可溶解49.7g碳酸钠(0℃时为7.0g,100℃为45.5g)。微溶于无水乙醇,不溶于丙醇。 CP2005关于药品的近似溶解度如下叙述: 极易溶解:系指溶质1g(ml)能在溶剂不到1ml中溶解; 易溶:系指溶质1g(ml)能在溶剂1~不到10ml中溶解; 溶解:系指溶质1g(ml)能在溶剂10~不到30ml中溶解; 略溶:系指溶质1g(ml)能在溶剂30~不到100ml中溶解; 微溶:系指溶质1g(ml)能在溶剂100~不到1000ml中溶解; 极微溶解:系指溶质1g(ml)能在溶剂1000~不到10000ml中溶解; 几乎不溶或不溶:系指溶质1g(ml)能在溶剂10000ml中不能完全溶解; 人们根据物质在20℃时的溶解度的大小,把它们在水中的溶解性分为以 下等级: 溶解度 >10克 >1克 <1克 <0.01克 溶解性易溶可溶微溶难溶 乙醇与水共沸点:78.17℃ 组成:乙醇96% 水4% (wt%)
高中化学常用物质溶解性表及沉淀颜色(xin)
高中化学常用物质溶解性表及沉淀颜色 钾、钠铵盐都可溶, 硝盐遇水影无踪; 硫(酸)盐不溶铅和钡, 氯(化)物不溶银、亚汞。 氢气应早去晚归,酒精灯迟到早退,试管口下倾水滴。 升失氧,降得还;若说剂,两相反。 无“弱”不水解,谁“弱”谁水解;愈“弱”愈水解, 又“弱”剧水解;谁“强”显谁性,双“弱”由K定。 左边水写分子式,中间符号写可逆,右边不写“↑”和“↓”。 钾钠铵盐溶水快,① 硫酸盐除去钡铅钙。② 氯化物不溶氯化银, 硝酸盐溶液都透明。③ 口诀中未有皆下沉。④ 注: ①钾钠铵盐都溶于水; ②硫酸盐中只有硫酸钡、硫酸铅、硫酸钙不溶; ③硝酸盐都溶于水; ④口诀中没有涉及的盐类都不溶于水;
钾、钠、铵盐、硝酸盐; 氯化物除银、亚汞; 硫酸盐除钡和铅; 碳酸、磷酸盐,只溶钾、钠、铵。 说明,以上四句歌谣概括了8类相加在水中溶解与不溶的情况。 钾钠铵硝皆可溶、盐酸盐不溶银亚汞; 硫酸盐不溶钡和铅、碳磷酸盐多不溶。 多数酸溶碱少溶、只有钾钠铵钡溶 钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。) 盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。) 再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。)其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物) 只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶) 最后说碱类,钾、钠、铵和钡。(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶) 另有几种微溶物,可单独记住。 钾钠铵盐硝酸盐 完全溶解不困难 氯化亚汞氯化银 硫酸钡和硫酸铅 生成沉淀记心间 氢硫酸盐和碱类 碳酸磷酸硝酸盐 可溶只有钾钠铵
钾、钠、硝酸溶,(钾盐、钠盐和硝酸盐都溶于水。) 盐酸除银(亚)汞,(盐酸盐里除氯化银和氯化亚汞外都溶。) 再说硫酸盐,不容有钡、铅,(硫酸盐中不溶的是硫酸钡和硫酸铅。) 其余几类盐,(碳酸盐、亚硫酸盐、磷酸盐、硅酸盐和硫化物) 只溶钾、钠、铵,(只有相应的钾盐、钠盐和铵盐可溶) 最后说碱类,钾、钠、铵和钡。(氢氧化钾、氢氧化钠、氢氧化钡和氨水可溶) 另有几种微溶物,可单独记住 高中化学常用物质溶解性表及沉淀颜色Fe2O3+3H2SO4= Fe2(SO4)3+3H2O 铁锈溶解溶液呈黄色铁器除锈 Al2O3+3H2SO4= Al2(SO4)3+3H2O 白色固体溶解 CuO+H2SO4=CuSO4+H2O 黑色固体溶解溶液呈蓝色 ZnO+H2SO4=ZnSO4+H2O 白色固体溶解 MgO+H2SO4=MgSO4+H2O 白色固体溶解 2NaOH+H2SO4=Na2SO4+2H2O Cu(OH)2+H2SO4=CuSO4+2H2O 蓝色固体溶解 Ca(OH)2+H2SO4=CaSO4+2H2O Mg(OH)2+H2SO4=MgSO4+2H2O 白色固体溶解 2Al(OH)3+3H2SO4=Al2(SO4)3+3H2O 白色固体溶解 2Fe(OH)3+3H2SO4=Fe2(SO4)3+3H2O 红褐色沉淀溶解溶液呈黄色 Ba(OH)2+ H2SO4=BaSO4+2H2O 生成白色沉淀不溶解于稀硝酸检验SO42的原理BaCl2+ H2SO4=BaSO4+2HCl 生成白色沉淀不溶解于稀硝酸检验SO42的原理Ba(NO3)2+H2SO4=BaSO4+2HNO3 生成白色沉淀不溶解于稀硝酸检验SO42的原 理 Na2O+2HNO3=2NaNO3+H2O 白色固体溶解 CuO+2HNO3=Cu(NO3)2+H2O 黑色固体溶解溶液呈蓝色 ZnO+2HNO3=Zn(NO3)2+ H2O 白色固体溶解 MgO+2HNO3=Mg(NO3)2+ H2O 白色固体溶解 CaO+2HNO3=Ca(NO3)2+ H2O 白色固体溶解 NaOH+HNO3=NaNO3+ H2O Cu(OH)2+2HNO3=Cu(NO3)2+2H2O 蓝色固体溶解 Mg(OH)2+2HNO3=Mg(NO3)2+2H2O 白色固体溶解 Al(OH)3+3HNO3=Al(NO3)3+3H2O 白色固体溶解 Ca(OH)2+2HNO3=Ca(NO3)2+2H2O Fe(OH)3+3HNO3=Fe(NO3)3+3H2O 红褐色沉淀溶解溶液呈黄色 3NaOH + H3PO4=3H2O + Na3PO4 3NH3+H3PO4=(NH4)3PO4 2NaOH+CO2=Na2CO3+ H2O 吸收COO2H2中的CO2 2NaOH+SO2=Na2SO3+ H2O 2NaOH+SO3=Na2SO4+ H2O 处理硫酸工厂的尾气 (SO2) FeCl3+3NaOH=Fe(OH)3+3NaCl 溶液黄色褪去有红褐色沉淀生成
常见物质的溶解性、颜色、俗称
常见物质的溶解性 1、气体:溶的:CO 2、HCl、SO2、NH3等。 不溶(或不易溶):O2、H2、CH4、CO、N2等。 2、金属氧化物:除CaO、Na2O、K2O、BaO溶外,大多数不溶 3、酸:大多数溶 4、碱:除氢氧化钡、氢氧化钾、氢氧化钙、氢氧化钠和氨水溶外,其他碱不溶于水; 5、盐:含有钾、钠、硝酸根、铵根的盐都溶于水; 含Cl-的盐只有AgCl不溶于水,其他都溶于水; 含SO42-的盐只有BaSO4不溶于水,其他都溶于水; 含CO32-的盐只有含K+、Na+、NH4+溶于水,其他都不溶于水。 酸碱盐溶解性口诀: 1、酸类多数都易溶; 2、碱类易溶钾钠钡铵,钙是微溶余不溶; 3、盐类: ①钾盐钠盐硝酸盐,还有铵盐都易溶;(钾钠铵硝都易溶) ②硫酸盐中钡不溶,硫酸钙银是微溶。 ③氯化物中银不溶; ④碳酸盐只溶钾钠氨,但是全能溶于酸。 ⑤AgCl、BaSO4遇酸也不溶,加稀硝酸不溶解。 常见物质的颜色 (一)固体的颜色 1、黑色固体:木炭C,氧化铜CuO,二氧化锰MnO2,四氧化三铁Fe3O4,铁粉Fe(铁块银白色) 2、紫黑色固体:高锰酸钾KMnO4 3、红色固体:铜Cu—紫红色,氧化铁Fe2O3——红(棕)色红磷P 4、红褐色沉淀:氢氧化铁Fe(OH)3 5、浅黄色固体:硫磺S 6、蓝色:硫酸铜晶体CuSO4·5H2O(无水硫酸铜白色),氢氧化铜沉淀Cu(OH)2 7、大部分固体:白色,如无水硫酸铜CuSO4,CaO,CaCO3 沉淀(即不溶于水的盐和碱): ①盐:白色↓:CaCO3、BaCO3(溶于酸)AgCl、BaSO4(也不溶于稀HNO3) 等; ②碱:蓝色↓:Cu(OH)2;红褐色↓:Fe(OH)3;白色↓:其余不溶性碱为白色。 (二)液体的颜色 1、大部分液体:无色,如水,稀盐酸,稀硫酸,酚酞试液等 2、蓝色溶液:含有Cu2+的溶液—硫酸铜Cu SO4溶液,氯化铜CuCl2溶液,硝酸铜Cu(NO3)2溶液 3、黄色溶液:含有Fe3+的溶液—Fe2(SO4)3溶液,FeCl3溶液,Fe(NO3)3硝酸铁溶液 4、浅绿色溶液:含有Fe2+的溶液—FeSO4溶液,FeCl2溶液,硝酸亚铁Fe(NO3)2溶液 5、紫红色溶液:高锰酸钾溶液KMnO4 6、紫色溶液:石蕊溶液 (三)常见气体、无色气体: 单质:氧气O2,氢气H2,氮气N2。 化合物:二氧化碳CO2,一氧化碳CO,甲烷CH4,氯化氢HCl,二氧化硫SO2。
沪教版九年级化学全册6.3.1 物质的溶解性学案
第6章 第三节 物质的溶解性(第1课时) 【学习目标】1.知道物质溶解性的涵义,通过探究记住影响物质溶解性的因素,并能解释生活中的 一些现象; 2.记住饱和溶液与不饱和溶液的概念,深刻理解影响溶液饱和与否的关键,会转化的 方法; 3.知道饱和与否与浓稀是两种不同的概念,两者只有在同种溶液同种温度下才能有关 联。 【学习重点】与物质溶解性有关的概念学习。 【学习难点】影响溶液饱和与否因素的掌握及相互转化方法的理解。 【学习过程】 一、回顾、预习与交流 【旧知回顾】: 1、(用 “难”、“不易”、“易”、“微”、“能”填空) H 2 溶于水, O 2 溶于水, CO 2 溶于水 NaCl 溶于水, CaCO 3 溶于水, Ca(OH)2 溶于水 2、除了水还有 可作溶剂。 3、举一个气体作溶质的溶液 (填溶液的名称)。 【新知导学】: 1、一定量水中能否无限制的溶解食盐?试画出下列有关图示曲线。 2、 称为 这种物质的溶解性。 二、合作、研讨与点拨 活动一、(一)影响物质溶解性的因素 1.阅读教材P16-17,完成实验1,实验2,实验3 实验1:溶质不同,溶剂相同 溶质(1g ) 食盐 蔗糖 氢氧化钙 溶剂(5mL ) 水 水 水 溶解情况 结论: 。 NaCl/g NaCl%
实验2:溶质相同,溶剂不同 结论:。 实验3:溶质、溶剂相同,温度不同 结论:。 小结:影响固体溶解性的因素、、。 2.实验4:打开雪碧瓶盖会有什么现象?如果加热会有什么现象? 结论:同种气体在同种溶剂中,压强减小,;温度升高,。思考:有人说可以将CO2大量储藏到深海中。为什么? 根据学过的知识,这种做法不可取。为什么? 小结:影响气体溶解性的因素 活动二、(二)饱和溶液、不饱和溶液 完成教材P17“活动与探究”,填写下表: 结论: (1)温度一定、水的量一定时,可溶解的KNO3的量。 (2)温度一定时,水量越多,溶解的KNO3。 (3)水的量一定时,温度升高,溶解的KNO3。 总结:,叫做这种溶质 ....的饱和溶液; 叫做这种溶质 ....的不饱和溶液。
初中化学_常见物质_溶解性表
阳离子 阴离子 OH—NO3—Cl—SO42—CO32— H+H 2O 溶.挥HNO3溶.挥HCl 溶H2SO4溶.挥H2CO3 NH 4+溶.挥NH 4OH 溶NH4NO3溶NH4Cl 溶(NH4)2SO4溶(NH4)2CO3 K+溶KOH 溶KNO 3溶KCl 溶K2SO4溶K2CO3 Na+溶NaOH 溶NaNO 3溶NaCl 溶Na2SO4溶Na2CO3 Ba2+溶Ba(OH) 2溶Ba(NO3)2溶BaCl2不BaSO4不BaCO3 Ca2+微Ca(OH) 2溶Ca(NO3)2溶CaCl2微CaSO4不CaCO3 Mg2+不Mg(OH) 2溶Mg(NO3)2溶MgCl2溶MgSO4微MgCO3 Al3+不Al(OH) 3溶Al(NO3)3溶AlCl3溶Al2(SO4)3---- Mn2+不Mn(OH) 2溶Mn(NO3)2溶MnCl2溶MnSO4不MnCO3 Zn2+不Zn(OH) 2溶Zn(NO3)2溶ZnCl2溶ZnSO4不ZnCO3 Fe2+不Fe(OH) 2溶Fe(NO3)2溶FeCl2溶FeSO4不FeCO3 Fe3+不Fe(OH) 3溶Fe(NO3)3溶FeCl3溶Fe2(SO4)3---- Cu2+不Cu(OH) 2溶Cu(NO3)2溶CuCl2溶CuSO4---- Ag+----溶AgNO 3不AgCl 微Ag2SO4不Ag2CO3 钾钠铵盐个个溶,硝酸盐类也相同 硫酸盐类除钡钙,卤盐除银和亚汞(氟除外) 碳磷酸盐多不溶,醋酸盐类全都溶 解化学计算题关键是读数据,读出每一个数据包含的物质,然后分析物质之间的关系,即可找出已知的量和物。 如:在一次化学课外活动中,某同学想除去氯化钾固体中混有的氯化铜(不引进其他杂质)。化学老师为他提供了以下溶液:氢氧化钠溶液、氢氧化钾溶液、硫酸钠溶液。该同学现取氯化钾和氯化铜的混合物59.8g,全部溶解在200g水中,再加入60g所选溶液,恰好完全反应,生成沉淀9.8g。试回答: (1)该同学所选的是溶液。 (2)计算混合物中氯化铜的质量和反应后所得溶液中溶质的质量分数。(结果保留到小数点后一位数字) 59.8g(氯化钾和氯化铜)+200g水+60g(氢氧化钾和水)=9.8g(氢氧化铜)是混合物的不能直接用于方程式计算,所以已知的是氢氧化铜的质量为9.8g,写出反应方程式就能计算了一.制氧气: 2KClO3 (MnO2,加热)= 2KCl + 3O2 ↑ 2KMnO4 加热=K2MnO4 + MnO2 + O2↑ 二.制氢气: Zn+2HCl=ZnCl+H2↑ Zn+H2SO4=ZNSO4+H2 ↑ 三.制二氧化碳: CaCO3+2HCl=CaCl2+CO2↑(不能用H2SO4) 20℃
