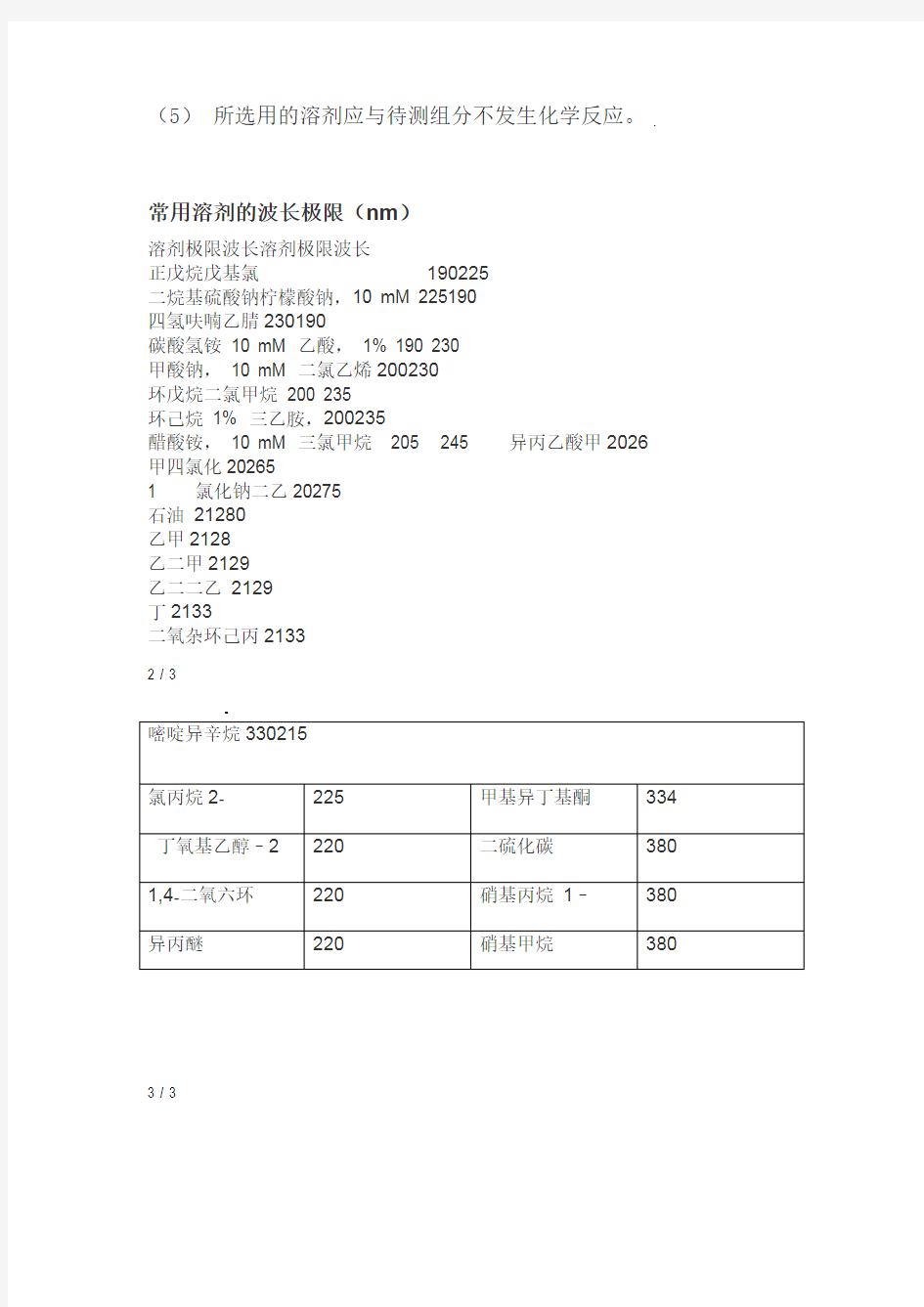
测定紫外光谱时溶剂的选择常用的溶剂的波长极限

.
测定紫外光谱时溶剂的选择(常用的溶剂的波长极限)
由于溶剂对电子光谱图的影响很大,因此在吸收光谱图上或数据表中必须注明所用溶剂;对已知化合物作紫外光谱比较时,也应注意所用溶剂是否相同。
紫外-可见分光光度法中如何正确选择溶剂?
溶剂极性除了对最大吸收峰波长有影响外,还影响吸收光谱的精细结构。当物质处于蒸气状态时,由于分子间的相互作用力减小到最低程度,电子光谱的精细结构(振转光谱)清晰可见;当物质处于非极性溶剂中时,由于溶质分子和溶剂分子间的相互碰撞,使精细结构部分消失;当物质处于极性溶剂中时,由于溶剂化作用,限制了分子的振动和转动,使精细结构完全消失,分子的电子光谱只呈现宽的谱线包封。测定化合物的紫外吸收光谱时选择溶剂的原则是:
(1)样品在溶剂中溶解良好,能达到必要的浓度以得到吸光度适中的吸收曲线;
(2)溶剂不影响样品的吸收光谱,因此在测定的波长范围内溶剂应当是紫外透明的,即溶解本身没有吸收。透明范围的最短波长称为透明界限,测试时应根据溶剂的透明界限选择合适的溶剂;
(3)为了降低溶剂与溶质分子间的作用力,减少溶剂对吸收光谱的影响,应尽量采用低极性溶剂;
1 / 3
.
(4)溶剂挥发性小、不易燃、无毒性、价格便宜;
(5)所选用的溶剂应与待测组分不发生化学反应。
常用溶剂的波长极限(nm)
溶剂极限波长溶剂极限波长
正戊烷戊基氯190225
二烷基硫酸钠柠檬酸钠,10 mM 225190
四氢呋喃乙腈230190
碳酸氢铵10 mM 乙酸,1% 190 230
甲酸钠,10 mM 二氯乙烯200230
环戊烷二氯甲烷200 235
环己烷1% 三乙胺,200235
醋酸铵,10 mM 三氯甲烷205 245 异丙乙酸甲2026甲四氯化20265
1 氯化钠二乙20275
石油21280
乙甲2128
乙二甲2129
乙二二乙2129
丁2133
二氧杂环己丙2133
2 / 3
.
3 / 3
常用溶剂的性质
常用溶剂的性质 常用溶剂的性质 常用溶剂的极性顺序:水(最大) >甲酰胺>乙腈>甲醇>乙醇>丙醇>丙酮>二氧六环>四氢呋喃>甲乙酮>正丁醇>乙酸乙酯>乙醚>异丙醚>二氯甲烷>氯仿>溴乙烷>苯>四氯化碳>二硫化碳>环己烷>己烷>煤油(最小)。 甲酰胺 分子式HCONH 2 ,透明油状液体,略有氨臭,具有吸湿性,可燃。能与水和乙醇混溶,微溶于苯、三氯甲烷和乙醚。相对密度1.133(20/4℃)。沸点210℃。熔点2.55℃。闪点175℃。折射率nD(25℃)1.4468。燃点>500℃。粘度(20℃)2.926mPa?s。 毒性本品低毒。对皮肤和粘膜有暂时刺激性。小鼠经口LD50大于1000mg/kg。 乙腈;甲基氰 结构式CH 3 CN。分子量41.05。无色透明液体,有醚的气味。相对密度(20℃/4℃)1. 7822,凝固点-43.8℃,沸点81.6℃、闪点5.6℃。折射率1.3441.粘度(20℃)0.35mPa?s,表面张力(20℃)19.10×10-3N/m,临界温度274.7℃,临界压力4.83MPa。能与水、甲醇、醋酸甲酯、醋酸乙酯、丙酮、乙醚、氯仿、四氯化碳、氯乙烯以及各种不饱和烃相混溶。与水形成共沸混合物。易燃,爆炸极限3.0%-16%(vol)。有毒人LD503800mg/kg。空气中最高容许浓度3mg/m3。贮存阴凉、通风、干燥的库房内,远离火种、热源,防止日光直射。 甲醇 结构式为CH 3 OH,分子量32.04。无色澄清易挥发液体,相对密度(20℃ /4℃)0.7914,凝固点-97.49℃,沸点64.5℃.闪点(开口)16℃,燃点470℃,折射率1.3285,表面张力22.55×10-3N/m,蒸气压(20 ℃)12.265kPa,蒸气相对密度1.11,粘度(20℃)0.5945mP a?s,溶解度参数δ=14.8,能与水、乙醇、乙醚、丙酮、苯、氯仿等有机溶剂混溶,甲醇对金属特别是黄铜有轻微的腐蚀性。易燃,燃烧时有无光的谈蓝色火焰。蒸气能与空气形成爆炸混合物.爆炸极限6.0%-36.5%(vol)。纯品略带乙醇味,粗品刺鼻难闻。有毒。饮用7-8g可导致失明,饮用30-100g就会死亡。空气中甲酵蒸气最高容许浓度5mg/m3。 乙醇 结构式为C 2H 5 OH,分子量46.07。无色透明液体,有酒的醉香气味,也有刺激性 的辛辣昧。工业乙醇含量为95%,相对密度(20℃/4℃)0.793。凝固点-114℃,沸点78.32℃,闪点(开口)16℃,燃点390-430 ℃.折射率1.3614,粘度(20℃)1.41mPa?s,表面张力(20℃)22.27×10-3N/m,比热容 (20 ℃)2.42kJ/(kgK),蒸气压(20 ℃)5.732kPa,溶解度参数δ=12.7。溶于苯、甲苯。与水、甲醇、乙醚、醋酸、氯仿任意比例混溶。能溶解许多有机化合物和若干无机化合物。与铬酸、次氯酸钙、过氧化氢、硝酸、硝酸铂、过氮酸盐及氧化剂反应剧烈,爆炸极限4.3%-19.0%(vol)。具有吸湿性,与水形成共沸混合物。微毒,有麻醉性,饮入乙醇中毒剂量75-80g。致死剂量为250-500g。空气中最高容许浓度1880mg/m3。
有机溶剂极性表
有机溶剂极性表
下图是混合有机溶剂极性顺序(由小到大,括号内表示的是混合比例) 强极性溶剂:甲醇〉乙醇〉异丙醇 中等极性溶剂:乙氰〉乙酸乙酯〉氯仿〉二氯甲烷〉乙醚〉甲苯 非极性溶剂:环己烷,石油醚,己烷,戊烷 常用混合溶剂: 乙酸乙酯/己烷:常用浓度0~30%。但有时较难在旋转蒸发仪上完全除去溶剂。 乙醚/戊烷体系:浓度为0~40%的比较常用。在旋转蒸发器上非常容易除去。乙醇/己烷或戊烷:对强极性化合物5~30%比较合适。 二氯甲烷/己烷或戊烷:5~30%,当其他混合溶剂失败时可以考虑使用。 3)将1~2mL选定的溶剂体系倒入展开池中,在展开池中放置一大块滤纸。 4)将化合物在标记过的基线处进行点样。我们用的点样器是买来的,此外,点样器也可从加热过的Pasteur吸管上拔下(你可以参照UROP)。在跟踪反应进行时,一定要点上起始反应物、反应混合物以及两者的混合物。 5)展开:让溶剂向上展开约90%的薄板长度。 6)从展开池中取出薄板并且马上用铅笔标注出溶剂到达的前沿位置。根据这个算Rf的数值。 7)让薄板上的溶剂挥发掉。 8)用非破坏性技术观察薄板。最好的非破坏性方法就是用紫外灯进行观察。将薄板放在紫外灯下,用铅笔标出所有有紫外活性的点。尽管在 5.301中不用这种方法,但我们将采用另一常用的无损方法--用碘染色法。(你可以参看UROP)。
9)用破坏性方式观测薄板。当化合物没有紫外活性的时候,只能采用这种方法。在 5.301中,提供了很多非常有用的染色剂。使用染色剂时,将干燥的薄板用镊子夹起并放入染色剂中,确保从基线到溶剂前沿都被浸没。用纸巾擦干薄板的背面。将薄板放在加热板上观察斑点的变化。在斑点变得可见而且背景颜色未能遮盖住斑点之前,将薄板从加热板上取下。 10)根据初始薄层色谱结果修改溶剂体系的选择。如果想让Rf变得更大一些,可使溶剂体系极性更强些;如果想让Rf变小,就应该使溶剂体系的极性减小些。如果在薄板上点样变成了条纹状而不是一个圆圈状,那么你的样品浓度可能太高了。稀释样品后再进行一次薄板层析,如果还是不能奏效,就应该考虑换一种溶剂体系。
常见的溶剂极性表有机溶剂表
常见的溶剂极性表有机溶剂表一般有机溶剂根据“相似相溶”的原理来进行选择 化合物名称极性粘度沸点吸收波长 i-pentane(异戊烷) 0 - 30 - n-pentane(正戊烷) 0 0.23 36 210 Petroleum ether(石油醚) 0.01 0.3 30~60 210 Hexane(己烷) 0.06 0.33 69 210 Cyclohexane(环己烷) 0.1 1 81 210 Isooctane(异辛烷) 0.1 0.53 99 210 Trifluoroacetic acid(三氟乙酸) 0.1 - 72 - Trimethylpentane(三甲基戊烷) 0.1 0.47 99 215 Cyclopentane(环戊烷) 0.2 0.47 49 210 n-heptane(庚烷) 0.2 0.41 98 200 Butyl chloride(丁基氯; 丁酰氯) 1 0.46 78 220 Trichloroethylene(三氯乙烯; 乙炔化三氯) 1 0.57 87 273 Carbon tetrachloride(四氯化碳) 1.6 0.97 77 265 Trichlorotrifluoroethane(三氯三氟代乙烷) 1.9 0.71 48 231 i-propyl ether(丙基醚; 丙醚) 2.4 0.37 68 220 Toluene(甲苯) 2.4 0.59 111 285 p-xylene(对二甲苯) 2.5 0.65 138 290 Chlorobenzene(氯苯) 2.7 0.8 132 - o-dichlorobenzene(邻二氯苯) 2.7 1.33 180 295 Ethyl ether(二乙醚; 醚) 2.9 0.23 35 220 Benzene(苯) 3 0.65 80 280 Isobutyl alcohol(异丁醇) 3 4.7 108 220 Methylene chloride(二氯甲烷) 3.4 0.44 240 245 Ethylene dichloride(二氯化乙烯) 3.5 0.78 84 228 n-butanol(正丁醇) 3.7 2.95 117 210 n-butyl acetate(醋酸丁酯;乙酸丁酯) 4 - 126 254 n-propanol(丙醇) 4 2.27 98 210 Methyl isobutyl ketone(甲基异丁酮) 4.2 - 119 330 Tetrahydrofuran(四氢呋喃) 4.2 0.55 66 220 Ethyl acetate(乙酸乙酯) 4.30 0.45 77 260 i-propanol(异丙醇) 4.3 2.37 82 210 Chloroform(氯仿) 4.4 0.57 61 245
常见有机溶剂极性表
有机溶剂是能溶解一些不溶于水的物质的一类有机化合物,其特点是在常温常压下呈液态,具有较大的挥发性,在溶解过程中,溶质与溶剂的性质均无改变。 有机溶剂的种类较多,按其化学结构可分为10大类:①芳香烃类:苯、甲苯、二甲苯等; ②脂肪烃类:戊烷、己烷、辛烷等;③脂环烃类:环己烷、环己酮、甲苯环己酮等;④卤化烃类:氯苯、二氯苯、二氯甲烷等;⑤醇类:甲醇、乙醇、异丙醇等;⑥醚类:乙醚、环氧丙烷等;⑦酯类:醋酸甲酯、醋酸乙酯、醋酸丙酯等;⑧酮类:丙酮、甲基丁酮、甲基异丁酮等;⑨二醇衍生物:乙二醇单甲醚、乙二醇单乙醚、乙二醇单丁醚等;⑩其他:乙腈、吡啶、苯酚等。 有机溶剂具有脂溶性,因此除经呼吸道和消化道进入机体内外,尚可经完整的皮肤迅速吸收,有机溶剂吸收入人体后,将作用于富含脂类物质的神经、血液系统,以及肝肾等实质脏器,同时对皮肤和粘膜也有一定的刺激性。不同有机溶剂其作用的主要靶器官和作用的强弱也不同,这决定于每一种有机溶剂的化学结构、溶解度、接触浓度和时间,以及机体的敏感性。 常用溶剂的极性顺序: 水(极性最大) > 甲酰胺 > 乙腈 > 甲醇 > 乙醇 > 丙醇 > 丙酮 > 二氧六环 > 四氢呋喃 > 甲乙酮 > 正丁醇 > 醋酸乙酯 > 乙醚 > 异丙醚 > 二氯甲烷 > 氯仿 > 溴乙烷 > 苯 > 氯丙烷 > 甲苯 > 四氯化碳 > 二硫化碳 > 环己烷 > 己烷 > 庚 烷 > 煤油(极性最小) 有机溶剂的极性根据官能团和对称性可初步判断,具体的需参照极性参数,如下
表示有机溶剂的极性,关系到其物理化学性质、如介电常数、偶极矩或折射率。这种表示方法把所有的溶剂看作是连续作用的介质,而不是看作由各个分子组成的非连续统一体,并且未考虑到溶剂和溶质之间的特殊的相互作用。
高效液相色谱
高效液相色谱 二、定义色谱法(Chromatography):利用组分在两相间分配系数不同而进行分离的技术。 *经验性学科色谱法的分离原理利用样品混合物中各组分理、化性质的不同以及在两相间分配系数的差异,当两相相对移动时各组分在两相中反复多次重新分配结果使混合物得到分离。 两相中固定不动的一相称固定相(Stationaryphase)移动的一相称流动相(Mobilephase)携带样品流过整个系统的流体。 色谱发展史◆年前俄国的植物学家Tswett创立了色谱法。 由Tswett创立的色谱法分离效率低分离时间长根据样品的不同一般分离需要几小时至几天。 ◆世纪年代至年代初先后出现了纸色谱(paperchromatography,PC)和薄膜色谱法(thinlayerchromatography,TLC)。 特点:较经典色谱法简单、分离时间短样品量要求小。 ◆年James和Martin提出了气相色谱法(gaschromatography,GC)特点:以气体作为流动相。 应用范围广泛受到人们重视。 但对不易气化和热不稳定性差的化合物难以分离。 ◆世纪年代后期由于新型色谱柱填料的高压输液泵和高灵敏度的检测器的出现发展出了高效液相色谱(Highperformanceliquidchromatography,HPLC)。
液相色谱:以液体作为流动相的色谱分离方法适用于高沸点、大分子、强极性和热稳定性差的化合物的分析流动相具有运载样品分子和选择性分离的双重作用*LCGCCE:泳毛细管电泳(capillaryelectrophoresis,CE)又叫高效毛细管电泳(HPCE),是近年来发展最快的分析方法之一。 SFC:supercriticalfluidchromatography超临界流体色谱。 一、液固吸附色谱(一)分离原理(二)常用吸附剂(三)吸附剂和流动相的选择经典液相色谱(一)分离原理各组分与流动相分子争夺吸附剂表面活性中心利用吸附剂表面的活性吸附中心对不同组分的吸附能力差异而实现分离(二)常用吸附剂:多孔、微粒状物质硅胶氧化铝聚酰胺硅胶结构:内部硅氧交联结构→多孔结构表面有硅醇基→氢键作用→吸附活性中心特性:)与极性物质或不饱和化合物形成氢键物质极性↑吸附能力↑→强极性吸附中心不易洗脱)吸水→失活→~OC烘干分钟(可逆失水)→吸附力最大→OC烘干(不可逆失水)→活性丧失无吸附力适用:分析酸性或中性物质氧化铝碱性氧化铝pH~适于分析碱性、中性物质中性氧化铝pH>适于分析酸性碱性和中性物质酸性氧化铝pH~适于分析酸性、中性物质聚酰胺氢键作用氢键能力↑强组分越后出柱(三)吸附剂和流动相的选择:依据被测组分、吸附剂和流动相的性质被测组分性质(极性大小):烃<<羧酸醇吸附剂的活性:吸附剂的活性↑大对被测组分的吸附能力↑强强极性物质选择弱吸附剂弱极性物质选择强吸附剂流动相的极性:流动相极性↑大对被测组分的洗脱能力↑大“相似相溶”原则:根据组
常用溶剂极性表
常用溶剂极性表
二:常用溶剂的沸点、溶解性和毒性 溶剂名称沸点℃(101.3kPa) 溶解性毒性 液氨-33.35 特殊溶解性:能溶解碱金属和碱土金属剧毒性、腐蚀性 液态二氧化硫-10.08 溶解胺、醚、醇苯酚、有机酸、芳香烃、溴、二硫化碳,多数饱和烃不溶剧毒 甲胺-6.3 是多数有机物和无机物的优良溶剂,液态甲胺与水、醚、苯、丙酮、低级醇混溶,其盐酸盐易溶于水,不溶于醇、醚、酮、氯仿、乙酸乙酯中等毒性,易燃 二甲胺7.4 是有机物和无机物的优良溶剂,溶于水、低级醇、醚、低极性溶剂强烈刺激性 石油醚不溶于水,与丙酮、乙醚、乙酸乙酯、苯、氯仿及甲醇以上高级醇混溶与低级烷相似 乙醚34.6 微溶于水,易溶与盐酸.与醇、醚、石油醚、苯、氯仿等多数有机溶剂混溶麻醉性 戊烷36.1 与乙醇、乙醚等多数有机溶剂混溶低毒性 二氯甲烷39.75 与醇、醚、氯仿、苯、二硫化碳等有机溶剂混溶低毒,
麻醉性强 二硫化碳46.23 微溶与水,与多种有机溶剂混溶麻醉,强刺激性 丙酮56.12 与水、醇、醚、烃混溶低毒,类乙醇,但较大 1,1-二氯乙烷57.28 与醇、醚等大多数有机溶剂混溶低毒、局部刺激性氯仿61.15 与乙醇、乙醚、石油醚、卤代烃、四氯化碳、二硫化碳等混溶中等毒性,强麻醉性 甲醇64.5 与水、乙醚、醇、酯、卤代烃、苯、酮混溶中等毒性,麻醉性四氢呋喃66 优良溶剂,与水混溶,很好的溶解乙醇、乙醚、脂肪烃、芳香烃、氯化烃吸入微毒,经口低毒 己烷68.7 甲醇部分溶解,比乙醇高的醇、醚丙酮、氯仿混溶低毒,麻醉性,刺激性 三氟代乙酸71.78 与水,乙醇,乙醚,丙酮,苯,四氯化碳,己烷混溶,溶解多种脂肪族,芳香族化合物 1,1,1-三氯乙烷74.0 与丙酮、甲醇、乙醚、苯、四氯化碳等有机溶剂混溶低毒 四氯化碳76.75 与醇、醚、石油醚、石油脑、冰醋酸、二硫化碳、氯代烃混溶氯代甲烷中,毒性最强 乙酸乙酯77.112 与醇、醚、氯仿、丙酮、苯等大多数有机溶剂溶解,能溶解某些金属盐低毒,麻醉性 乙醇78.3 与水、乙醚、氯仿、酯、烃类衍生物等有机溶剂混溶微毒类,麻醉性 丁酮79.64 与丙酮相似,与醇、醚、苯等大多数有机溶剂混溶低毒,毒性强于丙酮 苯80.10 难溶于水,与甘油、乙二醇、乙醇、氯仿、乙醚、、四氯化碳、二硫化碳、丙酮、甲苯、二甲苯、冰醋酸、脂肪烃等大多有机物混溶强烈毒性 环己烷80.72 与乙醇、高级醇、醚、丙酮、烃、氯代烃、高级脂肪酸、胺类混溶低毒,中枢抑制作用 乙睛81.60 与水、甲醇、乙酸甲酯、乙酸乙酯、丙酮、醚、氯仿、四氯化碳、氯乙烯及各种不饱和烃混溶,但是不与饱和烃混溶中等毒性,大量吸入蒸气,引起急性中毒 异丙醇82.40 与乙醇、乙醚、氯仿、水混溶微毒,类似乙醇 1,2-二氯乙烷83.48 与乙醇、乙醚、氯仿、四氯化碳等多种有机溶剂混溶高毒性、致癌 乙二醇二甲醚85.2 溶于水,与醇、醚、酮、酯、烃、氯代烃等多种有机溶剂混溶, 能溶解各种树脂,还是二氧化硫、氯代甲烷、乙烯等气体的优良溶剂吸入和经口低毒 三氯乙烯87.19 不溶于水,与乙醇、乙醚、丙酮、苯、乙酸乙酯、脂肪族氯代烃、汽油混溶有机有毒品 三乙胺89.6 水:18.7以下混溶,以上微溶, 易溶于氯仿、丙酮,溶于乙醇、乙醚易爆,皮肤黏膜刺激性强 丙睛97.35 溶解醇、醚、DMF、乙二胺等有机物,与多种金属盐形成加成有机物高毒性,与氢氰酸相似 庚烷98.4 与己烷类似低毒,刺激性、麻醉性 水100 略略
常用溶剂
按照溶剂墨水又可划分为:水性墨、油性墨。水性墨是以水和水溶性的溶剂作为溶解色基的主要成分的墨水。油性墨是以非水溶性的溶剂作为溶解色基的主要成分墨水。 具体的溶剂成分,按化学组成分类可分为:石油烃溶剂、煤焦溶剂、萜烃溶剂、醇类溶剂、酯类溶剂、酮类溶剂、醚酯类溶剂等。 给你介绍几种常用溶剂 1、松香水: 即200#溶剂汽油,它是石油的分留产物,可溶解松香、甘油硬脂和醇酸树脂,可调节金属、玻璃油墨,它的溶解力属中等范围,可与许多有机溶剂互溶。 2、松节油: 它是从松树提取的含油松脂的挥发部分。松节油有三种异构体:α-松萜、β-松萜、双戌烯。它蒸发均匀,由于分子结构中含有不饱和度,可产生氧化聚合作用,生成沉香萜醇溶于油和树脂中变为成膜物上的一个组份。松节油蒸发均匀,对氧化聚合型油墨有防止结皮并改善流平性的作用。 3、二甲苯: 工业用二甲苯是由邻位、间位、对位三种异物体的混合物。二甲苯溶解力比松节油、松香水大,挥发率比二者快,广泛应用于高温固化型油墨及氧化聚合型油墨中。 4、甲苯: 它来源于石油化工或煤焦工业,甲苯能溶解乙基纤维素、顺酐树脂、橡胶、过氯乙烯等,可调节玻璃油墨、金属油墨。 5、乙醇: 根据用途不同,它的纯度不同,无水乙醇的纯度为99.5%,工业乙醇为95.6%,医药乙醇为70~75%。乙醇可溶解许多天然树脂,如:虫胶、聚醋酸乙烯、环己酮树脂、聚乙烯醇缩醛树脂(网印制版用粘网胶就是用它配制的),但乙醇对耐溶剂的感光胶有破坏作用。 6、二丙酮醇: 易分解、分解主要产物是丙酮,它能溶解松香、聚醋酸乙烯、硝酸纤维、虫胶、氯醋共聚树脂等。 7、丙酮: 它是极易挥发的有机液体,可溶解过氯乙烯树脂、氯醋共聚树脂、氯化橡胶等。它对耐溶
常用有机溶剂分类
有机溶剂分类 一、烃类溶剂 1.烃 只含有碳氢两种元素的有机化合物叫烃。根据结构将烃类分为脂肪烃和芳香烃。脂肪烃包括脂肪链烃和脂环烃。开链结构的脂肪烃根据结构的饱和程度分为饱和链烃(烷烃)和不饱和链烃(烯烃和炔烃)。芳香烃是含有苯环特殊结构的烃类。根据具体结构分为单环芳烃、多环芳烃和稠环芳烃。 烃类溶剂根据来源分为两类:由石油分馏得到的烃类混合物溶剂叫石油溶剂油,简称溶剂油;由化工原料合成或精制得到的成分单一烃类溶剂是烃的纯溶剂。纯溶剂价格较高,通常只用于一些特殊用途中。 2.溶剂油 石油是由多种烃类组成的混合物,经过分馏处理得到不同沸点范围的产品。根据沸,抿范围通常把石油产品分为石油醚、汽油、煤油、柴油、润滑油、石蜡和沥青。其中沸点范围在30~90℃以戊烷和己烷为主要成分的石油醚和沸点范围在40~200℃烃分子含碳数在4~12的汽油,有很好的溶解性能。在工业生产中常做溶剂使用,称为溶剂油或溶剂汽油。近年来还开发出相当于煤油乃至轻柴油馏分做高沸点溶剂油,拓宽了溶剂油的概念。煤油是石油分馏时,沸点在175~325℃范围的馏分,由于馏程长所包含的烃类成分复杂。在一定情况下也可以做溶剂使用,如美国干洗业使用的干洗溶剂汽油(stoddard solvent)实际上是一种不易燃的煤油溶剂。因此广义上溶剂油包括多种沸程范围的烃类混合物以及己烷、苯、甲苯、二甲苯纯烃类溶剂。为了叙述上的方便,本书介绍的溶剂油是指由石油分馏得到的烃类混合物溶剂。 (1)溶剂油按沸程分类根据分馏过程的沸程,溶剂油大致分为三类:把沸程在100℃凋以下的称为低沸点溶剂油,如工业上的6号抽提溶剂油,沸程为60~90℃;把沸程在100~150℃的称为中沸点溶剂油,如橡胶溶剂油,沸程在80~120℃;把沸程高于150℃的称为高调沸点溶剂油,如油漆溶剂油,沸程为140—200℃,油墨溶剂油干点达360℃都属于高沸点溶剂油。从沸程范围看,溶剂油大多数属于汽油馏分。 (2)溶剂油的化学成分溶剂油是各种烃类的混合物,主要成分有开链烷烃、烯烃、环烷烃和芳香烃。由于烯烃化学性质活泼、安定性差,不适合作溶剂使用,所以一般溶剂油中含烯烃很少,成分以其他三类烃为主。 低沸程溶剂油,如6号抽提溶剂油,120号橡胶溶剂油,200号油漆溶剂油中主要成分是烷烃和环烷烃。有时称为脂肪烃类溶剂,脂肪烃溶剂油成分有直链烷烃、支链烷烃、环烷烃。由于不同结构烷烃的溶解性能不同,所以又可以根据其主要成分进一步分类,如以支链烷烃为主要成分的溶剂油,称为异构烷烃溶剂油,它的溶解性能优于一般脂肪烃溶剂油而高沸程溶剂油中甲苯、二甲苯等芳烃含量较大称为芳烃类溶剂油,如近年兴起的高沸点芳烃溶剂油主要成分就是分子中含9个碳原子的芳烃。 溶剂油的性能与其化学成分有密切关系,由于烃类的溶解能力顺序为:芳烃>环烷烃> 链烷烃。所以相同沸程的溶剂油中含链烷烃、环烷烃多的比含芳烃较多的溶剂油苯胺点高、贝壳松脂丁醇值低,溶解能力差。 纯芳香烃溶剂油虽然溶解能力强,但毒性也大,因此目前工业上出现用高芳香烃溶剂油和低芳香烃溶剂油来代替苯、甲苯、二甲苯等纯芳香烃溶剂使用的趋势。这样虽然溶解能力稍有降低,但降低了溶剂油的毒性,也降低了生产成本。而且为降低溶剂油的毒性,各国对溶剂油中的芳香
常见溶剂的极性大小
常用溶剂极性2007年04月29日星期日19:35在结晶和重结晶纯化化学试剂的操作中,溶剂的选择是关系到纯化质量和回收率的关键问题。选择适宜的溶剂时应注意以下几个问题:1. 选择的溶剂应不与欲纯化的化学试剂发生化学反应。例如脂肪族卤代烃类化合物不宜用作碱性化合物结晶和重结晶的溶剂;醇类化合物不宜用作酯类化合物结晶和重结晶的溶剂,也不宜用作氨基酸盐酸盐结晶和重结晶的溶剂。 2. 选择的溶剂对欲纯化的化学试剂在热时应具有较大的溶解能力,而在较低温度时对欲纯化的化学试剂的溶解能力大大减小。 3. 选择的溶剂对欲纯化的化学试剂中可能存在的杂质或是溶解度甚大,在欲纯化的化学试剂结晶和重结晶时留在母液中,在结晶和重结晶时不随晶体一同析出;或是溶解度甚小,在欲纯化的化学试剂加热溶解时,很少在热溶剂溶解,在热过滤时被除去。 4. 选择的溶剂沸点不宜太高,以免该溶剂在结晶和重结晶时附着在晶体表面不容易除尽。 用于结晶和重结晶的常用溶剂有:水、甲醇、乙醇、异丙醇、丙酮、乙酸乙 酯、氯仿、冰醋酸、二氧六环、四氯化碳、苯、石油醚等。此外,甲苯、硝基甲烷、乙醚、二甲基甲酰胺、二甲亚砜等也常使用。二甲基
甲酰胺和二甲亚砜的溶解能力大,当找不到其它适用的溶剂时,可以试用。但往往不易从溶剂中析出结晶,且沸点较高,晶体上吸附的溶剂不易除去,是其缺点。乙醚虽是常用的溶剂,但是若有其它适用的溶剂时,最好不用乙醚,因为一方面由于乙醚易燃、易爆,使用时危险性特别大,应特别小心;另一方面由于乙醚易沿壁爬行挥发而使欲纯化的化学试剂在瓶壁上析出,以致影响结晶的纯度。 在选择溶剂时必须了解欲纯化的化学试剂的结构,因为溶质往往易溶于与其结构相近的溶剂中―“相似相溶”原理。极性物质易溶于极性溶剂,而难溶于非极性溶剂中;相反,非极性物质易溶于非极性溶剂,而难溶于极性溶剂中。这个溶解度的规律对实验工作有一定的指导作用。如:欲纯化的化学试剂是个非极性化合物,实验中已知其在异丙醇中的溶解度太小,异丙醇不宜作其结晶和重结晶的溶剂,这时一般不必再实验极性更强的溶剂,如甲醇、水等,应实验极性较小的溶剂,如丙酮、二氧六环、苯、石油醚等。适用溶剂的最终选择,只能用试验的方法来决定。下表可供选择溶剂时参考。 物质的类别溶解度大的溶剂 烃疏水性烃、醚、卤代烃 卤代烃 醚 胺 酯酯
常用有机溶剂极性表
微波化学-溶剂极性 1.前言:只有极性物质能吸收微波,非极性物质不吸收微波,一般介电常数e>15者,称之为极性溶剂,在进行实验时,务必确保反应的试剂中含有极性物质。而介电常数e<15者决不能单独作为反应样品进行微波加热,否则会造成磁控管打火,烧坏仪器。如果试验中所用试剂为非极性时,在不影响实验的情况下,应该混合加入极性溶剂或者极性物质以利反应,如:碳化硅 2.常用有机溶剂的极性表 溶剂介电常数(e) 溶剂介电常数(e) 溶剂介电常数(e) 三甲基苯 1.90 丁酸乙酯 5.10 甲丙酮16.80 环己烷 2.02 溴苯 5.17 苯乙酮17.30 四氯化碳 2.24 丁胺 5.40 苯甲醛17.80 1,2-二氧六环 2.25 丁酸甲酯 5.60 丁醇17.80 苯 2.30 氯苯 5.62 异丙醇17.90 对二甲苯 2.30 苯甲酸乙酯 6.02 环己酮18.20 三甲苯 2.30 乙酸乙酯 6.02 苯乙腈18.30 二甲苯 2.40 乙酸 6.15 丁酮18.50 甲苯 2.40 乙胺 6.30 异丁醇18.70 三乙胺 2.42 乙酸甲酯 6.70 丙酮20.70 萘 2.50 甲酸乙酯7.10 丁腈20.70 7.20 乙酸酐21.00 三甲胺 2.50 1,2-二甲氧基乙 烷 邻二甲胺 2.57 苯胺7.30 甲醛23.00 二硫化碳 2.60 四氢呋喃7.58 酒精24.30 己酸 2.60 正丁醇7.80 乙醇24.50 戊酸 2.60 2,2,2-三氟乙醇8.55 苯甲腈26.00 乙醛 2.90 三氟乙酸8.55 乙二腈27.00 正丁酸 2.90 二氯乙烷8.93 丙腈27.70 丁酸 3.00 邻二氯苯9.93 甲醇32.70 呋喃 3.00 1,2-二氯乙烷10.36 硝基苯34.82 乙苯 3.00 2-甲基2-丙醇10.90 硝基甲烷35.87 36.70 丙酸 3.10 丁酸酐12.00 N,N-二甲基甲 酰胺 丁醚 3.10 吡啶12.50 乙二醇37.00 辛酸 3.20 苯甲醇13.00 乙腈37.50 三氯乙烯 3.40 二苯甲酮13.00 N,N-二甲基乙37.80
HPLC色谱常见问题
指的是流动相在紫外短波段的吸收。描述一种溶剂的末端吸收常用其截止波长描述。 溶剂的紫外截止波长指当小于截止波长的辐射通过溶剂时,溶剂对此辐射产生强烈吸收,此时溶剂被看作是光学不透明的,它严重干扰组分的吸收测量。 其测量是将溶剂装入1cm的比色皿,以空气为参比,逐渐降低入射波长,溶剂的吸光度A=1时的波长称为溶剂的截止波长。也称极限波长。 中国药典对UV法溶剂的要求是:以空气为空白,溶剂和吸收池的吸收度在220~240nm范围内不得超过0.40,在241~250nm范围内不得过0.20,在251~300nm 范围内不得过0.10,在300nm以上不得过0.05。 末端吸收简单的说就是紫外吸收短波端有强而不成峰值吸收处,简单的一个例子就是你很可能都见到过一个物质紫外扫描图谱中小于200nm的地方就是强吸收,但没有吸收峰 出现倒峰的原因,以下是查到的一些资料: 1.常为溶剂峰,流动相的紫外吸收大于样品的溶剂的紫外吸收,就产生倒峰. 2.样品中的杂质没有紫处吸收或吸收很小,而流动相紫外吸收大,如用甲醇时波长设定在220nm以下时,常出现这种现象. 3.进样过程中进入了空气也会导致的. 4.如果流动相有紫外吸收的杂质,使用紫外检测器时,会产生倒峰,必须用高纯度的溶剂作为流动相。 5.检测器的极性接反了,也会出现倒峰 从液相色谱的角度来解释,出现倒峰一般是分析物的吸收比流动相的吸收还要小, HPLC色谱常见问题 1.用HPLC进行分析时保留时间有时发生漂移,有时发生快速变化,原因何在?如何解决? 2.液相色谱中峰出现拖尾或出现双峰的原因是什么? 3.HPLC灵敏度不够的主要原因及解决办法 4.做HPLC分析时,柱压不稳定,原因何在?如何解决? 5.我最近更换了另一种牌号的ODS柱,虽然分离情况仍可以,但保留时间不重现,为什么? 6.我购买的HPLC柱验收测试时柱压过高,请问为什么? 7.色谱双峰产生的可能及判断和处理 8.色谱柱中的流动相会排干吗? 9.使用PEEK(polyetheretherketone)管路和接头需要注意什么问题? 10.液相色谱梯度洗脱中柱温的影响有那些? 11.为何基线会漂移 12.规则的基线噪音是如何产生的
常用溶剂极性表
溶剂极性表
ethanol 4.30 1.20 79 210 Ethyl acetate 乙酸乙酯 4.30 0.45 77 260 i-propanol(丙醇) 4.30 2.37 82 210 Chloroform(氯仿) 4.40 0.57 61 245 Methyl ethyl ketone(甲基乙 4.50 0.43 80 330 基酮) Dioxane( 二恶烷; 二氧六 4.80 1.54 102 220 环; 二氧杂环己烷) Pyridine(吡啶) 5.30 0.97 115 305 Acetone(丙酮) 5.40 0.32 57 330 Nitromethane(硝基甲烷) 6.00 0.67 101 380 Acetic acid(乙酸) 6.20 1.28 118 230 0.37 82 210 Acetonitrile(乙腈) 6.20 Aniline(苯胺) 6.30 4.40 184 -- Dimethyl formamide(二甲 6.40 0.92 153 270 基甲酰胺) Methanol(甲醇) 6.60 0.60 65 210 Ethylene glycol(乙二醇) 6.90 19.90 197 210 Dimethyl sulfoxide() 7.20 2.24 189 268 water 10.20 1.00 100 268 水(最大) > 甲酰胺> 乙腈> 甲醇> 乙醇> 丙醇> 丙酮> 二氧六环> 四氢呋喃> 甲乙酮> 正丁醇> 乙酸乙酯> 乙醚> 异丙醚> 二氯甲烷>氯仿>溴乙烷>苯>四氯化碳>二硫化碳>环己烷>己烷>煤油(最小) 溶剂选择的三条通用规律可以遵循。1、极性相似原则。即极性相近的物质可以互溶。如汽车漆中极性比较高的氨基漆一般选择极性比较高的丁醇等做溶剂。2、溶剂化原则。溶剂化是指溶剂分子对溶质分子产生的相互作用,当作用力大于溶质分子的内聚力时,便使溶质分子彼此分开而溶于溶剂中。如极性分子和聚合物的极性基团相互吸引而产生溶剂化作用,使聚合物溶解。3、溶解度参数原则。即如果溶剂的溶解度参数和聚合物的溶解度参数相近或相等时,就能使这一聚合物溶解,应用此原则较易掌握,还可用于电子计算机进行选择。 溶剂化原则: 极性高分子溶解在极性溶剂中的过程,是极性溶剂分子(含亲电基团或亲核基团)和高分子的(亲核或亲电)极性基团相互吸引产生溶剂化作用,使高分子溶解。溶剂化作用是放热的。因而对于有这些基团的聚合物,要选择相反基团的溶剂。比如尼龙6 是亲核的,要选择甲酸、间甲酚等带亲电基团的溶剂;相反聚氯乙烯是亲电的,要选择环己酮等带亲核基团的溶剂。 高分子和溶剂中常见的亲核或亲电基团,按其从强到弱顺序排列如下:亲电基团:- SO3H, -COOH, -C6H4OH, =CHCN, =CHNO2, -CHCl2, =CHCl 亲核基团:-CH2NH2, - C6H4NH2, -CON(CH3)2, -CONH-, ≡PO4, -CH2COCH2-, -CH2OCOCH2-, -CH2OCH2- 非极性高分子与溶剂的越接近,越易溶解。一般认为 <1.7~2 可以溶解。 主要可以用以下三种间接的方法求得: (1)黏度法,使高分子溶液有最大特性黏数的溶剂的对应于高分子的。
几种常用溶剂的物理性质
丙酮 物理性质 丙酮结构式[2] 外观与性状:无色透明易流动液体,有芳香气味,极易挥发。 熔点(℃):-94.6 相对密度(水=1):0.80 沸点(℃):56.5 相对蒸气密度(空气=1):2.00 分子式:C3H6O 分子量:58.08 饱和蒸气压(kPa):53.32(39.5℃) 燃烧热(kJ/mol):1788.7 临界温度(℃):235.5 临界压力(MPa):4.72 辛醇/水分配系数的对数值:-0.24 闪点(℃):-20
爆炸上限%(V/V):13.0 引燃温度(℃):465 爆炸下限%(V/V):2.5 溶解性:与水混溶,可混溶于乙醇、乙醚、氯仿、油类、烃类等多数有机溶剂。 正己烷 物化性质 【熔点(℃)】-95.3 【沸点(℃)】68.74 【闪点(℃)】-23 【密度(D.)】:0.692 g/mL at 20 ℃[2] 【爆炸下限%(VN)】1.2% 【爆炸上限%(VN)】7.4% 【性状】有微弱的特殊气味的无色挥发性液体。 【溶解性】不溶于水,可与乙醚、氯仿、乙醇混溶,溶于丙酮,与甲醇不互溶 甲醇 理化性质编辑 物理性质 物态液体 颜色透明,无色 气味纯品清淡,类似乙醇;粗品刺激难闻熔点-98 °C(lit.)
沸点64.5~64.7 °C(lit.)密度0.791 g/mL at 25 °C 闪点52 °F(约11°C)蒸气密度 1.11 (大气压=1) log P(辛醇/水分配系数)-0.69[4] 蒸气压127 mm Hg(25°C)[5] 410 mm Hg(50°C)折射率n20/D 1.329(lit.)爆炸上限%(V/V):44.0 爆炸下限%(V/V): 5.5 沾染量<10(APHA) 水溶解性易溶 储存条件室温 水 物理 水 通常是无色、无味的液体。 沸点:100℃(气压为一个标准大气压时)。 凝固点:0℃ 三相点:0.01℃
Solvent-UV-cutoff溶剂截止波长
Solvent Cut-off wavelengths Solvents L0/nm L1/nm 1,2,4-trichlorobenzene 350 1,2-dichlorobenzene 350 295 1,2-dichloroethane 250 230 1,2-dimethoxyethane 300 220 2,2,4-trimethylpentane 230 210 2-ethoxyethanol 280 210 2-methoxyethanol 270 200 2-propanol 240 205 4-methylpentanone 375 335 5-methylhexanone 350 330 acetone 340 330 acetonitrile 200 190 benzene 295 280 butan-2-one 345 330 chlorobenzene 310 285 chloroform 260 240 cyclohexane 235 200 cyclopentane 220 195 decalin 250 230 dichloromethane 245 230 diethyl ether 255 220 dimethylsulphoxide 330 285 ethanol 240 205 ethyl acetate 280 260 heptane 230 200 hexane 225 195 isobutanol 250 200
methanol 240 205 n-butanol 245 215 n-butyl acetate 275 255 nitromethane >400 380 NN-dimethylformamide 300 270 n-propanol 250 210 o-xylene 325 290 p-dioxane 290 220 pentane 230 200 Pyridine 345 325 s-butanol 285 260 tetrachloroethylene 320 290 tetrahydrofuran 280 220 toluene 315 285 trichloroethylene >400 water 190 185 In this table, approximate wavelengths (nm) are specified below which the solvent absorbance may be unacceptable. For quantitative work, the cut-off may be set at a wavelength (L0) where the absorbance for 10 nm pathlength of the solvent exceeds 0.05 absorbance units (relative to water), i.e. A1cm>0.05. For qualitative work, it may still be feasible to work at significantly lower wavelengths and most analysts accept a cut-off based on the wavelength (L1) for A1cm > 1.0.
展开剂的选择以及常用溶剂极性表
展开剂的选择以及常用溶剂极性表 选择适当的展开剂是首要任务.一般常用溶剂按照极性从小到大的顺序排列大概为:石油迷<己烷<苯<乙醚Petroleumether/Ethylacetate,petroleumether/Acetone,Petroleumether/Ether, Petroleumether/CH2Cl2, ethylacetate/MeOH,CHCl3/ethylacetate 展开剂的比例要靠尝试.一般根据文献中报道的该类化合物用什么样的展开剂,就首先尝试使用该类展开剂,然后不断尝试比例,直到找到一个分离效果好的展开剂。展开剂的选择条件:①对的所需成分有良好的溶解性;②可使成分间分开;③待测组分的Rf在~之间,定量测定在~之间;④不与待测组分或吸附剂发生化学反应;⑤沸点适中,黏度较小;⑥展开后组分斑点圆且集中;⑦混合溶剂最好用新鲜配制。 一般来说,弱极性溶剂体系的基本两相由正己烷和水组成,再根据需要加入甲醇、乙醇,乙酸乙酯来调节溶剂系统的极性,以达到好的分离效果,适合于生物碱、黄酮、萜类等的分离;中等极性的溶剂体系由氯仿和水基本两相组成,由甲醇、乙醇,乙酸乙酯等来调节,适合于蒽醌、香豆素,以及一些极性较大的木脂素和萜类的分离;强极性溶剂,由正丁醇和水组成,也靠甲醇、乙醇,乙酸乙酯等来调节,适合于极性很大的生物碱类化合物的分离。 很多时候,展开剂的选择要靠自己不断变换展开剂的组成来达到最佳效果。我们在实验中,为了实现一个配体与其他杂质有效分离,曾经尝试了很多种的溶剂组合,最后才找到石油醚—EtOAc—HCOOH(::)混合溶剂。一般把两种溶剂混合时,采用高极性/低极性的体积比为1/3的混合溶剂,如果有分开的迹象,再调整比例(或者加入第三种溶剂),达到最佳效果;如果没有分开的迹象(斑点较“拖”),最好是换溶剂。对于在硅胶中这种酸性物质上易分解的物质,在展开剂里往往加一点点三乙胺,氨水,吡啶等碱性物质来中和硅胶的酸性。(选择所添加的碱性物质,还必须考虑容易从产品中除去,氨水无疑是较好的选择。)分离效果的好坏和所用硅胶和溶剂的质量很有关系:不同厂家生产的硅胶可能含水量以及颗粒的粗细程度,酸性强弱不同,从而导致产品在某个厂家的硅胶中分离效果很好,但在另一个厂家的就不行。溶剂的含水量和杂质含量对分离效果都有明显的影响。温度,湿度对分离效果影响也很明显,在实验中我们发现有时同一展开条件,上下午的Rf截然不同 展开剂的选择主要根据样品的极性、溶解度和吸附剂的活性等因素来考虑 在进行薄层层析时,首先应该知道未知化学成分的类型,其极性的大致归属,从提取液或从色谱柱的流动相极性可知,另外某样品里含多种化学成分先按极性不同大致分,然后细分,对于分离未知的化学物质,展开剂的选择也是一个摸索的过程,不应该仅仅从展开剂考虑,多因素综合衡量! 溶剂:层析过程中溶剂的选择,对组分分离关系极大。在柱层析时所用的溶剂(单一剂或混合溶剂)习惯上称洗脱剂,用于薄层或纸层析时常称展开剂。洗脱剂的选择,须根据被分离物质与所选用的吸附剂性质这两者结合起来加以考虑在用极性吸附剂进行层析时,当被分离物质为弱极性物质,一般选用弱极性溶剂为洗脱剂;被分离物质为强极性成分,则须选用极性溶剂为洗脱剂。如果对某一极性物质用吸附性较弱的吸附剂(如以硅藻土或滑石粉代替硅
常用溶剂特性
常用溶剂特性 化工涂料知识2009-12-02 14:23:18 阅读174 评论0 字号:大中小 化学品中文名称:苯 化学品英文名称:benzene 技术说明书编码:233 CAS No.:71-43-2 分子式:C6H6 分子量:78.11 主要成分:纯品 外观与性状:无色透明液体,有强烈芳香味。 熔点(℃): 5.5 沸点(℃):80.1 相对密度(水=1):0.88 相对蒸气密度(空气=1): 2.77 饱和蒸气压(kPa):13.33(26.1℃) 燃烧热(kJ/mol):3264.4 临界温度(℃):289.5 临界压力(MPa): 4.92 辛醇/水分配系数的对数值: 2.15 闪点(℃):-11 引燃温度(℃):560 爆炸上限%(V/V):8.0 爆炸下限%(V/V): 1.2 溶解性:不溶于水,溶于醇、醚、丙酮等多数有机溶剂。 主要用途:用作溶剂及合成苯的衍生物、香料、染料、塑料、医药、炸药、橡胶等。 化学品中文名称:甲苯 化学品英文名称:methylbenzene 英文名称2:Toluene 技术说明书编码:306 CAS No.:108-88-3 分子式:C7H8 分子量:92.14 主要成分:纯品 外观与性状:无色透明液体,有类似苯的芳香气味。 熔点(℃):-94.9 沸点(℃):110.6 相对密度(水=1):0.87 相对蒸气密度(空气=1): 3.14 饱和蒸气压(kPa):4.89(30℃) 燃烧热(kJ/mol):3905.0 临界温度(℃):318.6
临界压力(MPa): 4.11 辛醇/水分配系数的对数值: 2.69 闪点(℃): 4 引燃温度(℃):535 爆炸上限%(V/V):7.0 爆炸下限%(V/V): 1.2 溶解性:不溶于水,可混溶于苯、醇、醚等多数有机溶剂。 主要用途:用于掺合汽油组成及作为生产甲苯衍生物、炸药、染料中间体、药物等的主要原料。 化学品中文名称:二氯甲烷 化学品英文名称:dichloromethane 技术说明书编码:753 CAS No.:75-09-2 分子式:CH2Cl2 分子量:84.94 主要成分:含量: 工业级一级≥99.0%; 二级≥98.0%。 外观与性状:无色透明液体,有芳香气味。 熔点(℃):-96.7 沸点(℃):39.8 相对密度(水=1): 1.33 相对蒸气密度(空气=1): 2.93 饱和蒸气压(kPa):30.55(10℃) 燃烧热(kJ/mol):604.9 临界温度(℃):237 临界压力(MPa): 6.08 辛醇/水分配系数的对数值: 1.25 闪点(℃):无资料 引燃温度(℃):615 爆炸上限%(V/V):19 爆炸下限%(V/V):12 溶解性:微溶于水,溶于乙醇、乙醚。 主要用途:用作树脂及塑料工业的溶剂。 化学品中文名称:1,4-二甲苯 化学品英文名称:1,4-xylene 中文名称2:对二甲苯 英文名称2:p-xylene 技术说明书编码:117 CAS No.:106-42-3 分子式:C8H10 分子量:106.17 主要成分:含量≥99.2%。 外观与性状:无色透明液体,有类似甲苯的气味。
